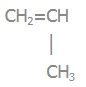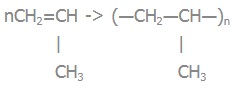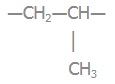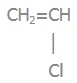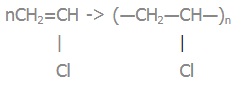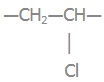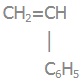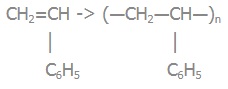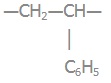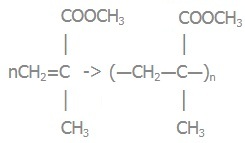ЗАВДАННЯ ДЛЯ САМОКОНТРОЛЮ
Вправа 1 Що таке синтетичнi полiмери? Це продукти органiчного синтезу із речовин неполiмерної будови
Вправа 2 Яка відмінність між реакціями полімеризації та поліконденсації?
Реакція поліконденсації різниться тим, що вона відбувається з утворенням побічного продукту, яким найчастіше буває вода або інша низькомолекулярна сполука
Вправа 3 Пояснiть вплив структури полiмерiв на їxнi фiзичнi властивостi.
Полімери лінійної будови (наприклад, поліетилен низького тиску, целюлоза) — еластичні, гнучкі, термопластичні, розчиняються з утворенням в'язких розчинів.
Полімери розгалуженої будови (наприклад, поліетилен високого тиску, поліпропілен) — нееластичні, гнучкі (чим нижчий ступінь розгалуженості, тим більш гнучкі), термопластичні, погано розчиняються.
Полімери просторової, або сітчастої будови (наприклад, фенолформальдегідні смоли, вулканізований каучук, гума) — пружні, легко руйнуються, термореактивні, набрякають у розчинниках, не розчиняючись.
Вправа 4 На якi групи подiляють полiмери за вiдношенням до нагрiвання?
На термопластичні і термореактивні
Вправа 5 Що таке пластмаси? Матеріали на основі полімерів, містять наповнювачі, пігменти та інші сипкі компоненти
Вправа 6 Назвiть основнi галузi застосування пластмас. Техніка, сільське господарство, побут
Вправа 7 Схарактеризуйте вiдомi вам полiмери, з яких виготовляють пластмаси (мономер, реакцiя добування, мономерна ланка).
1) поліетилен:
| Мономер: СН2=СН2 етилен (етен) |
| Реакція полімеризації: nCH2=CH2 -> (―CH2―CH2―)n |
| Мономерна ланка: ―CН2―CН2― |
2) поліпропілен:
|
Мономер:
пропілен (пропен) |
|
Реакція полімеризації:
|
|
Мономерна ланка:
|
3) поліхлоровініл:
|
Мономер:
хлоровініл |
|
Реакція полімеризації:
|
|
Мономерна ланка:
|
4) поліcтирен, або полістерол:
|
Мономер:
cтирен |
|
Реакція полімеризації:
|
|
Мономерна ланка:
|
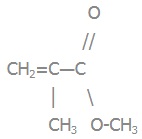
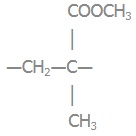
5) полiметилметакрилат:
|
Мономер:
метиловий естер метакрилової кислоти |
|
Реакція полімеризації:
|
|
Мономерна ланка:
|
6) тефлон:
|
Мономер: CF2=СF2 1,1,2,2-тетрафлуороетен |
| Реакція полімеризації: nCF2=CF2 -> (―CF2―CF2―)n |
| Мономерна ланка: ―СF2―CF2― |
Вправа 8 Схарактеризуйте полiетилен високого i низького тиску. Полiетилен низького тиску (0,2—2,5 МПа, 80—100°С) має лiнiйну структуру, молекули в масi полiмеру щiльно упакованi, через те зростає ступiнь кристалiчностi. Полiетилен високого тиску (150—300 МПа, 200—280°С) має розгалужену структуру
Вправа 9 Полiпропiлен стереорегулярної будови — кристалiчна, високоплавка речовина, що утворює мiцнi волокна, а нестереорегулярний полiмер м’який, еластичний. Пояснiть це з погляду тeopiї будови. Молекули в масі поліпропілену стереорегулярної будови щільно упаковані, тому він перебуває у кристалічному стані, а нестереорегулярний полімер — в аморфному стані
Додаткове завдання
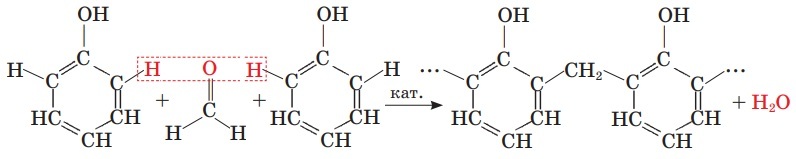
Складiть рiвняння послiдовних реакцiй, за допомогою яких можна добути бакелiт, виходячи з коксу.
Добування фенолу:
С + 2H2 -> CH4
2CH4 -> C2H2 + 3H2 (при 15000С)
3C2H2 -> C6H6 (при 6500С)
C6H6 + Cl2 -> C6H5Cl + HCl (при кат.)
C6H5Cl + NaOH = C6H5OH + NaCl (при t0C, кат.)
Добування метаналю:
CH4 + Cl2 -> CH3Cl + HCl (при hv)
CH3Cl + H2O -> CH3OH + HCl (при t0C, кат.)
CH3OH + CuO -> HCHO + Cu + H2О
Поліконденсація бакеліту: