Електронегативність — це умовна величина, яка характеризує здатність атомів елемента відтягувати до себе електрони, що беруть участь в утворенні хімічних зв’язків.
Електронегативність хімічного елемента можна оцінити кількісно. Відповідні обчислення були здійснені за результатами фізичних досліджень атомів.
Найчастіше використовують шкалу електронегативності
американського науковця Лайнуса Полінга.
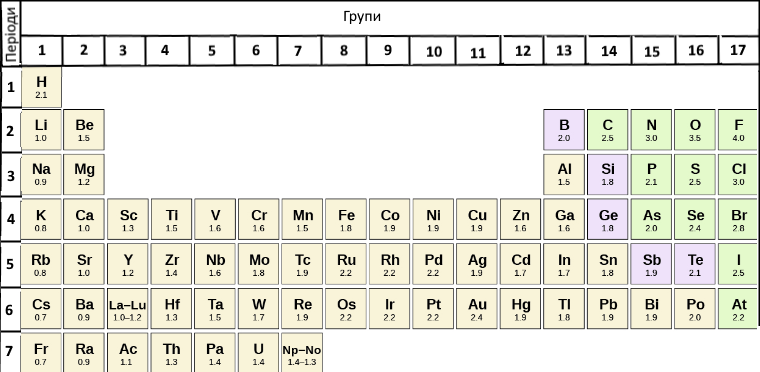
Оскільки електронегативність — це властивість, яка пов'язана з прийманням і втратою електронів, то й змінюватися вона буде так само, як і неметалічні властивості: у періодах електронегативність посилюється зліва направо, а в групах — знизу догори. Отже, найбільш електронегативним елементом є Флуор (4.0), а найменш електронегативними — Цезій та Францій (0.7).
Що менший радіус атома і більший заряд його ядра, то сильніше атом притягує спільну пару електронів.
З урахуванням електронегативності укладено ряд електронегативності хімічних елементів, в якому кожний наступний хімічний елемент характеризується меншою електронегативністю за попередній:

Отже, Флуор — «абсолютний чемпіон» з електронегативності. Друге місце посідає Оксиген, третє — Хлор, четверте — Нітроген. Загалом неметалічні елементи мають значно більшу електронегативність, ніж металічні.