Другие задания смотри здесь...
![]()
Контрольные вопросы
Вопрос 1 Каким способом можно определить количественный состав веществ? По химической формуле можно определить соотношение масс атомов разных химических элементов в веществе и вычислить массовую долю элемента в веществе.
Вопрос 2 Как определяется массовая доля элемента в веществе? Приведите формулу для ее вычисления. Ее вычисляют как отношение атомной массы данного элемента с учетом числа его атомов в молекуле к относительной молекулярной массе вещества:
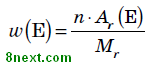
где w(E) — массовая доля химического элемента E, выраженная в долях единицы;
n — число атомов элемента E, обозначенное индексом в формуле соединения;
Ar — относительная атомная масса элемента E;
Mr — относительная молекулярная масса вещества.
Вопрос 3 Какова физическая суть понятия «массовая доля элемента в веществе»? Физическая суть массовой доли заключается в том, что она показывает массу атомов данного элемента в 100 г вещества
Вопрос 4 Выберите правильные утверждения:
а) по химической формуле можно узнать, какие химические элементы входят в состав вещества;
б) по химической формуле можно узнать соотношение атомов разных элементов в веществе;
в) по химической формуле можно узнать, сколько атомов каждого элемента входит в состав молекулы вещества;
г) по химической формуле можно узнать форму молекулы вещества.
Ответ: а), б), в)
Вопрос 5 Выберите правильный ответ. Массовая доля элемента в веществе показывает:
а) во сколько раз масса одного атома больше массы молекулы;
б) массу атомов данного химического элемента в 100 г вещества;
в) отношение массы атомов данного химического элемента к молекулярной массе;
г) сколько атомов каждого элемента входит в состав молекулы.
Ответ: б)
Задания для усвоения материала
Упражнение 1 Вычислите массовые доли всех элементов в соединениях со следующими химическими формулами:
а) NO2;
Mr(NO2) = Ar(N)+2•Ar(O)=14+2•16=46
w(N)= Ar(N)/Mr(NO2)=14:46=0,304, или 30,4%
Массовую долю Оксигена можно найти так:
w(О)=1-ω(N)=1-0,304=0,696, или 69,6%
или так:
w(О)=100%-ω(N)=100%-30,4%=69,6%
либо так:
w(О)=2•Ar(О)/Mr(NO2)=2•16:46=0,696
Ответ: w(N)=0,304, или 30,4%; w(О)=0,696, или 69,6%
б) PbCl2;
Mr(PbCl2)=Ar(Pb)+2•Ar(Cl)=207+2•35,5=278
w(Pb)=Ar(Pb)/Mr(PbCl2)=207:278=0,745, или 74,5%
w(Cl)=1-w(Pb)=1-0,745=0,255, или 25,5%
Ответ: w(Pb)=0,745, или 74,5%; w(Cl)=0,255, или 25,5%
в) Na2CO3;
Mr(Na2CO3)=2•Ar(Na)+Ar(C)+3•Ar(O)=2•23+12+3•16=106
w(Na)=2•Ar(Na)/Mr(Na2CO3)=2•23:106=0,434, или 43,4%
w(C)=Ar(C)/Mr(Na2CO3)=12:106=0,113, или 11,3%
w(O)=1-w(Na)-w(C)=1-0,434-0,113=0,453, или 45,3%
Ответ: w(Na)=0,434, или 43,4%; w(C)=0,113, или 11,3%,
w(O)=0,453, или 45,3%
г) H2SO4;
Mr(H2SO4)=2•Ar(H)+Ar(S)+4•Ar(O)=2•1+32+4•16=98
w(H)=2•Ar(H)/Mr(H2SO4)=2•1:98=0,02, или 2%
w(S)=Ar(S)/Mr(H2SO4)=32:98=0,327, или 32,7%
w(O)=1-w(H)-w(S)=1-0,02-0,327=0,653, или 65,3%
Ответ: w(H)=0,02, или 2%; w(S)=0,327, или 32,7%,
w(O)=0,653, или 65,3%
д) Ba3(PO4)2.
Mr(Ba3(PO4)2)=3•Ar(Ba)+2•Ar(P)+8•Ar(O)=3•137+2•31+8•16=601
w(Ba)=3•Ar(Ba)/Mr(Ba3(PO4)2)=3•137:601=0,684, или 68,4%
w(P)=2•Ar(P)/Mr(Ba2(PO4)2)=2•31:601=0,103, или 10,3%
w(O)=1-w(Ba)-w(P)=1-0,684-0,103=0,213, или 21,3%
Ответ: w(Ba)=0,684, или 68,4%; w(S)=0,103, или 10,3%,
w(O)=0,213, или 21,3%
Упражнение 2 Формула глюкозы C6H12O6, формула сахарозы C12H22O11. В каком веществе массовая доля Оксигена больше?
Вычислим массовые доли Оксигена в глюкозе и сахарозе.
Mr(С6Н12O6)=6•Ar(С)+12•Ar(Н)+6•Ar(O)=6•12+12•1+6•16=180
w1(О)=6•Ar(О)/Mr(С6Н12О6)=6•16:180=0,533, или 53,3%
Mr(С12Н22O11)=12•Ar(С)+22•Ar(Н)+11•Ar(O)=12•22+22•1+11•16=342
w2(О)=11•Ar(О)/Mr(С12Н22О11)=11•16:342=0,515, или 51,5%
51,5% <53,3%
Ответ: массовая доля Оксигена больше в глюкозе.
Упражнение 3 Вычислите массу атомов Гидрогена, которые содержатся в аммиаке NH3 массой 10 г.
Дано: m(NH3)=10 г
Найти: m(H)-?
Роешение:
І способ
1. Вычислим массовую долю Гидрогена в аммиаке NH3:
Mr(NH3)=Ar(N)+3•Ar(H)=14+3•1=17
w(H)=3•Ar(H)/Mr(NH3)=3•1:17=0,176, или 17,6%
2. Массовая доля элемента показывает часть массы вещества, приходящуюся на данный элемент. Вычислим массу атомов Гидрогена в воде массой 10 г:
m(H)=w(Н)•m(NH3)=0,176•10 г=1,76 г
ІІ способ
1. Вычислим массовую долю Гидрогена в аммиаке NH3:
Mr(NH3)=Ar(N)+3•Ar(H)=14+3•1=17
w(H)=3•Ar(H)/Mr(NH3)=3•1:17=0,176, или 17,6%
2. Массовая доля показывает массу атомов данного элемента в 100 г вещества.
В 100 г аммиака содержится 17,6 г Гидрогена,
в 10 г аммиака ― х г Гидрогена.
100 г / 10 г = 17,6 г / х г
х г • 100 г = 17,6 г • 10 г
х = 17,6 г • 10 г : 100 г
х = 1,76 г
Ответ: m(H)=1,76 г.
Упражнение 4 Масса воды на Земле оценивается приблизительно в 1,45•1018 тонн. Вычислите, какая масса атомов Гидрогена и Оксигена содержится в этой массе воды.
Дано: m(H2O)=1,45•1018 т
Найти: m(H)-?, m(O)-?
Решение:
І способ
Вычислим массовую долю Гидрогена и Оксигена в воде:
Mr(H2О)=2•Ar(H)+Ar(O)=2•1+16=18
w(H)=2•Ar(H)/Mr(H2О)=2•1:18=0,111, или 11,1%
w(О)=Ar(О)/Mr(H2О)=16:18=0,889, или 88,9%
Массовая доля элемента показывает часть массы вещества, приходящуюся на данный элемент. Вычислим массу атомов Гидрогена и Оксигена в воде массой 1,45•1018 т:
m(H)=w(Н)•m(H2О)=0,111•1,45•1018 т≈1,61•1017 т
m(О)=w(О)•m(H2О)=0,889•1,45•1018 т≈1,29•1018 т
ІІ способ
Вычислим массовую долю Гидрогена и Оксигена в воде:
Mr(H2О)=2•Ar(H)+Ar(O)=2•1+16=18
w(H)=2•Ar(H)/Mr(H2О)=2•1:18=0,111, или 11,1%
w(О)=Ar(О)/Mr(H2О)=16:18=0,889, или 88,9%
Массовая доля показывает массу атомов данного элемента в 100 г вещества.
В 100 г воды содержится 11,1 г Гидрогена,
в 1,45•1024 г воды ― х г Гидрогена.
100 г / 1,45•1024 т = 11,1 г / х г
х г • 100 г = 1,45•1024 г • 11,1 г
х = 1,45•1024 т • 11,1 г : 100 г
х = 0,161•1024 г=1,61•1023 г=1,61•1017 т
В 100 г воды содержится 88,9 г Оксигена,
в 1,45•1024 г воды ― х г Оксигена.
100 г / 1,45•1024 г = 88,9 г / х г
х г • 100 г = 1,45•1024 г • 88,9 г
х = 1,45•1024 г • 88,9 г : 100 г
х = 1,29•1024 г=1,29•1018 т
Ответ: m(H)=1,61•1017 т, m(О)=1,29•1018 т.