![]()
Упражнение 46 Атом элемента 2-го периода имеет на последнем энергетическом уровне 6 электронов. Сколько среди них спаренных электронов, а сколько неспаренных? 4 спаренных и 2 неспаренных
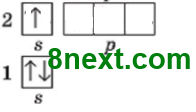
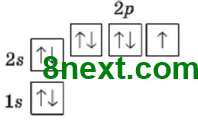
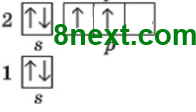
Этим атомом является Оксиген, электронная формула которого 1s22s22p4, а графическая имеет вид:

С шести електронов на внешнем (2) энергетическом уровне есть два s-електроны, которые являются спаренными и 4 р-электроны, из них, 2 р-электроны спаренные и 2 р-электроны неспаренные, вместе есть 4 спаренных и 2 неспаренных электрона.
Упражнение 47 В атомах каких элементов 2-го периода находится один неспаренный электрон, два неспаренных электрона?
Один неспаренный электрон:
|
Литий 1s22s1
|
Бор 1s22s22p1
|
Флуор F 1s22s22p5
|
Два неспаренных електрона:
|
Карбон 1s22s12p2
|
Оксиген 1s22s22p4
|
Упражнение 48 Назовите элемент, атом которого имеет такую электронную формулу:
а) 1s2; Гелий
б) 1s22s22p63s1; Натрий
в) [He]2s22p5; Флуор
г) [Ne]3s1. Натрий
Объяснение.
а) сумма электронов в записи электронной формулы атома элемента численно равна его порядковому номеру, поэтому находим сумму электронов и определяем соответствующий элемент. Всего 2 s-электрона, поэтому №2 — это Гелий;
б) сумма электронов в записи электронной формулы атома элемента численно равна его порядковому номеру, поэтому находим сумму электронов и определяем соответствующий элемент. Всего 11 электронов, поскольку 1s22s22p63s1 : 2+2+6+1=11, №11 — это Натрий.
в) електронная формула внешнего энергетического уровня ...2s22p5. Заполняется второй уровень, поэтому элемент расположен во 2-м периоде. На внешнем уровне в него 2+5=7 электронов, следовательно элемент расположен в VІІ группе, это р-элемент, поэтому — в главной подгруппе. Ищем в Периодической системе клетку на пересечении 2-го периода и VII группы. Этот элемент — Флуор;
г) електронная формула внешнего энергетического уровня ...3s1. Заполняется третий уровень, поэтому элемент расположен в 3-м периоде. На внешнем уровне в него 1 электрон, следовательно элемент расположен в І группе, это s-элемент, поэтому — в главной подгруппе. Ищем в Периодической системе клетку на пересечении 3-го периода и I группы. Этот элемент— Натрий.
Упражнение 49 Назовите два элемента, в атомах которых количество всех s- и всех р-электронов одинаковое.
Оксиген 1s22s22p4 имеет 4 s-электрона и 4 р-электрона
Магний 1s22s22p63s2 имеет 6 s-электронов и 6 р-электронов
Упражнение 50 Какое значение валентности может иметь элемент, если его атом имеет электронную формулу:
а) 1s22s22p63s23p3; Три
На внешнем (3) энергетическом уровне есть 2 s-электроны, которые являются спаренными, и 3 р-электроны, которые являются неспаренными, а на возможное значение валентности элемента указывает количество неспаренных электронов в его атоме, поэтому возможна валентность три.
б) [Ne]3s23p5? Один
На внешнем (3) энергетическом уровне есть 2 s-электроны, которые являются спаренными, и 5 р-электронов, из них, 4 р-электроны спаренные и 1 р-электрон неспаренный, а на возможное значение валентности элемента указывает количество неспаренных электронов в его атоме, поэтому возможна валентность один.