![]()
Упражнение 79 Что общего в электронном строении атомов инертных элементов? Атомы инертных элементов на внешнем энергетическом уровне содержат восемь электронов (исключение Гелий — два электрона).
Упражнение 80 Какая частица содержит больше электронов:
а) атом или соответствующий катион; Атом
Катион — это заряженная частица, которая образуется из атома вследствие потери им электрона.
б) атом или соответствующий анион? Анион
Анион — это заряженная частица, которая образуется из атома вследствие присоединения ним электрона.
Упражнение 81 Какие из элементов — Rb, Br, Sr, N — способны образовывать катионы, а какие — анионы? Определите заряд иона каждого элемента и напишите химические формулы этих частиц.
|
Катион Rb+ |
Анион Br- | Катион Sr2+ | Анион N3- |
Элементы Rb и Sr металлические, атомы которых содержат на внешнем энергетическом уровне 1 и 2 электрона соответственно, а атомы металлических элементов имеют на внешнем энергетическом уровне небольшое количество электронов (как правило, от 1 до 3) и способны терять их, превращаясь в катионы.
Запишем схему преобразования этих атомов на катионы и электронные формулы частиц:
Rb – e– → Rb+;
атом Rb — 1s22s22p63s23p64s23d104p65s1, или [Kr]5s1
ион Rb+ — 1s22s22p63s23p64s23d104p6, или [Kr]
Sr – 2e– → Sr2+;
атом Sr — 1s22s22p63s23p64s23d104p65s2, или [Kr]5s2
ион Sr2+ — 1s22s22p63s23p64s23d104p6, или [Kr]
Элементы Br и N неметаллические, атомы которых содержат на внешнем энергетическом уровне 7 и 5 электронов соответственно, а атомы неметаллических элементов (кроме инертных) имеют на внешнем энергетическом уровне от 4 до 7 электронов и способны присоединять дополнительные электроны, превращаясь в анионы.
Запишем схему преобразования этих атомов на анионы и электронные формулы частиц:
Br + e– → Br-;
атом Br — 1s22s22p63s23p64s23d104p5, или [Ar]4s23d104p5
ион Br- — 1s22s22p63s23p64s23d104p6, или [Kr]
N + 3e– → N3-;
атом N — 1s22s22p3, или [He]2s23p3
ион N3- — 1s22s22p6, или [Ne]
Упражнение 82 Составьте электронные формулы ионов Be2+, P3–, F– и K+.
| Ион |
Электронные формулы |
|
Ве2+ |
1s2, или [He] |
|
Р3- |
1s22s22p63s23р6, или [Ar] |
|
F-
|
1s22s22p6, или [Ne] |
|
K+ |
1s22s22p63s23p6, или [Ar] |
Упражнение 83 Назовите три катиона и два аниона, электронное строение которых такое же, как и иона F–.
| Катионы: Na+, Mg2+, Al3+ | Анионы: N3-, O2- |
Ион F- имеет электронное строение 1s22s22s6, или [Ne] — это могут быть катионы атомов металлических элементов, содержащихся в 3 периоде или анионы атомов неметаллических элементов (кроме инертных), содержащихся во 2 периоде периодической системы.
Упражнение 84 Какой атом имеет такое же электронное строение, что и ион Алюминия? Атом Неона
Напишите электронную формулу частицы и изобразите ее графический вариант.
Электронная формула иона Алюминия 1s22s22p6, или [Ne]
Графическая формула иона Алюминия:
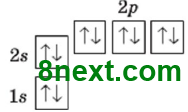
Упражнение 85 Напишите химические формулы частиц, у которых электронное строение внешнего энергетического уровня — 3s23p6.
Такое електроное строение внешнего уровня ...3s23р6 имеет атом Аргона, поэтому это могут быть катионы атомов металлических элементов, содержащихся в 4 периоде и анионы атомов неметаллических элементов, содержащихся в 3 периоде периодической системы.
| Ar | K+ | Ca2+ | Si4- | P3- | S2- | Cl- |
Упражнение 86 В атоме какого элемента содержится на 2 электрона меньше, чем в ионе Магния? В атома Оксигена
Запишем электронное строение иона Магния 1s22s22p6
С электронной формулы видим, что ион Mg2+ содержит 10 электронов (2+2+6=10), а атом неизвестного элемента должен содержать 8 (10-2=8) электронов, а значит и протонов, то есть иметь порядковый №8. Этим элементом является Оксиген.
Упражнение 87 Составьте электронную формулу частицы, которая имеет 16 протонов и 18 электронов.
1s22s22p63s23p6, или [Ar]
Назовите эту частицу. Анион Сульфура S2-
На число протонов указывает порядковый номер элемента, поэтому этим атомом является Сульфур (№16). Число электронов на 2 больше, чем протонов, следовательно, атом принял два электрона и превратился в анион с зарядом -2.
атом S — 1s22s22p63s23p4, или [Ne]3s23p4
ион S2- — 1s22s22p63s23p6, или [Ar]
Упражнение 88 Напишите схемы образования катиона и аниона Гидрогена из атома.
Атом Н - е- -> Н+ катион
Атом Н + е- -> Н- анион
Какая частица имеет наименьший радиус — катион, анион или атом Гидрогена? Катион Гидрогена
Почему? Размер радиуса зависит от числа энергетических уровней и количества электронов, а катион Гидрогена — это заряженная частица, которая образуется из атома вследствие потери им электрона. Радиус катиона Н+ меньше, а радиус аниона Н- почти не отличается от радиуса атома Гидрогена.
Упражнение 89 Укажите в приведенном перечне частицы с наибольшим и наименьшим радиусами: атом Ar, ионы K+, Са2+, Сl–. С наибольшим радиусом ион Cl-, с найменьшим — ион Са2+
Ответ обоснуйте. Радиус катиона меньший, а радиус аниона почти не отличается от радиуса соответствующего атома.