Пригадай із курсу хімії за 7 клас
• Поясни, як обчислюють масові частки компонентів суміші на прикладі суміші 5 г крохмалю і 15 г борошна.
Очислюють масу суміші (5 г +15 г = 20 г).
Визначають масову частку крохмалю в суміші (5 г : 20 г = 0,25, або 25%).
Визначають масову частку борошна в суміші (15 г : 20 г = 0,75, або 75%).
Обчисли масову частку кухонної солі у 50 г її водного розчину, для виготовлення якого використали 6 г солі.
Відомо: m(розчину) = 50 г, m(солі)=6 г
Знайти: w(солі) – ?
Розв'язання
w(солі) = m(солі):m(розчину)= 6 г : 50 г = 0,12, або 12%
Відповідь: масова частка солі 12%.
Завдання 1
На основі наведеної вище інформації виберіть закінчення речення: «Масова частка елемента показує ...»
А масу атомів усіх хімічних елементів у сполуці
Б масу атомів одного хімічного елемента у сполуці
В частку хімічного елемента у сполуці
Г співвідношення мас елементів у сполуці
Для підвищення врожайності культурних рослин городники вносять у ґрунт мінеральні добрива. Важливим джерелом Нітрогену, який необхідний для фотосинтезу та росту рослин, є натрієва селітра NaNO3 і калієва селітра KNO3. Яке з цих добрив потрібно внести в ґрунт у меншій кількості для забезпечення рослин однаковою кількістю Нітрогену? У меншій кфлькості потрібно внести в грунт калієву селітру KNO3, бо масова частка Нітрогену в цьому добриві більша.
Завдання 3
Використайте дані таблиці 8 і з’ясуйте, внесення якого добрива для забезпечення рослин Нітрогеном буде дешевшим.
| Вага | Вартість | |
| Калієва селітра | 1 кг | 87 грн |
| Натрієва селітра | 25 кг | 2750 грн |
Розв'язання
2750 : 25 = 110 (грн) – ціна натрієвої селітри.
87 грн < 110 грн
Відповідь: калієва селітра дешевша.
Завдання 1
Для виготовлення лікарських настоянок, як компонент палива для двигунів внутрішнього згорання, у косметиці й харчовій промисловості використовують етанол С2Н5ОН.
Склади характеристику етанолу за планом.
1. Якісний і кількісний склад молекули.
Молекула етанолу складається з 2 атомів Карбону, 6 атомів Гідрогену, 1 атом Оксигену.
2. Відносна молекулярна маса.
Мr(С2Н5ОН) = 2Аr(С) + 6Ar(H)+ Аr(O)=2•12+6•1+16=24+6+16=46
3. Масові частки хімічних елементів в етанолі.
w(C) = 2Ar(C):Mr(C5H5OH)= 24 : 46 = 0,52, або 52%
w(H) = 6Ar(H):Mr(C5H5OH)= 6 : 46 = 0,13, або 13%
w(O) = Ar(O):Mr(C5H5OH)= 16 : 46 = 0,35, або 35%
Завдання 2
Визнач масові частки елементів у сульфатній кислоті, модель молекули якої зображено.
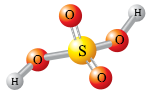
План виконання цього завдання.
1. Обчислюємо відносну молекулярну масу сульфатної кислоти.
Мr(H2SO4) = 2Аr(H) + Ar(S)+ 4Аr(O)=2•1+32+4•16=2+32+64=98
2. Обчислюємо масові частки хімічних елементів в сульфатній кислоті.
w(H) = 2Ar(H):Mr(H2SO4)= 2 : 98 = 0,02, або 2%
w(S) = Ar(S):Mr(H2SO4)= 32 : 98 = 0,327, або 32,7%
w(O) = 4Ar(O):Mr(H2SO4)= 64 : 98 = 0,653, або 65,3%
Завдання 3
Одним із видів газового пального для автомобілів є пропан. Це легкозаймиста речовина, молекула якої складається з трьох атомів Карбону і восьми атомів Гідрогену.
| Хімічна формула | Mr | Масові частки хімічних елементів |
| C3H8 | 44 |
81,9% Карбону 18,1% Гідрогену |
ТОБІ ДО СНАГИ
Завдання 1
Обчисли масові частки елементів в ортофосфатній кислоті H3PO4.
Відомо: сполука H3PO4
Знайти: w(H) – ?, w(P) – ?, w(O) – ?
Розв'язання
1. Обчислюємо відносну молекулярну масу сполуки.
Mr(H3PO4) = 3Ar(H) + Ar(P) + 4Ar(O) = 3 + 31 + 64 = 98
2. Обчислюємо масові частки елементів.
w(H) = 3Ar(H) : Mr(H3PO4) = 3 : 98 = 0,031, або 3,1%
w(P) = Ar(P) : Mr(H3PO4) = 31 : 98 = 0,316, або 31,6%
w(O) = 4Ar(O) : Mr(H3PO4) = 64 : 98 = 0,653, або 65,3%
Відповідь: w(H) = 3,1%, w(P) = 31,6%, w(O) = 65,3%.
Завдання 2
Визнач масову частку (%) металічного елемента в кальцій сульфаті CaSO4.
Відомо: сполука CaSO4
Знайти: w(Ca) – ?, w(S) – ?, w(O) – ?
Розв'язання
1. Обчислюємо відносну молекулярну масу сполуки.
Mr(CaSO4) = Ar(Ca) + Ar(S) + 4Ar(O) = 40 + 32 + 64 = 136
2. Обчислюємо масові частки елементів.
w(Ca) = Ar(Ca) : Mr(CaSO4) = 40 : 136 = 0,294, або 29,4%
w(S) = Ar(S) : Mr(CaSO4) = 32 : 136 = 0,235, або 23,5%
w(O) = 4Ar(O) : Mr(CaSO4) = 64 : 136 = 0,471, або 47,1%
Відповідь: w(Ca) = 29,4%, w(S) = 23,5%, w(O) = 47,1%.
Завдання 3
Розташуй хімічні формули СuS, FeCl2, MgO, AlH3 за зростанням масової частки неметалічного елемента у речовинах.
1. Обчислюємо відносні молекулярні маси речовин.
Mr(CuS) = Ar(Cu) + Ar(S) = 64 + 32 = 96
Mr(FeCl2) = Ar(Fe) + 2Ar(Cl) = 56 + 71 = 127
Mr(MgO) = Ar(Mg) + Ar(O) = 24 + 16 = 40
Mr(AlH3) = Ar(Al) +3Ar(H) = 27 + 3 = 30
2. Обчислюємо масові частки неметалічних елементів.
w(S) = Ar(S) : Mr(CuS) = 32 : 96 = 0,334, або 33,4%
w(Cl) = 2Ar(Cl) : Mr(FeCl2) = 71 : 127 = 0,559, або 55,9%
w(O) = Ar(O) : Mr(MgO) = 16 : 40 = 0,4, або 40%
w(H) = 3Ar(H) : Mr(AlH3) = 3 : 30 = 0,1, або 10%
Відповідь: AlH3, CuS, MgO, FeCl2.
Завдання 4
Монета номіналом 50 копійок важить 4,2 г. Масова частка Алюмінію у монеті становить 9 %. Обчисли масу алюмінію в десяти таких монетах.
Відомо: m(монети) = 4,2 г, w(Al) = 9%
Знайти: m(Al) – ?, маса алюмінію в 10 монетах?
Розв'язання
1. Обчислюємо масу алюмінію в монеті.
m(Al) = m(монети) • w(Al) : 100% = 4,2 г • 9% : 100% = 0,378 г
2. Обчислюємо масу алюмінію в десяти таких монетах.
0,378 г • 10 = 3,78 г
Відповідь: в десяти таких монетах 3,78 г алюмінію.
Завдання 5
Поміркуй і не здійснюючи математичних дій, дай відповідь на запитання: «У якій речовині — карбон (ІІ) оксиді чи кальцій оксиді — масова частка Оксигену більша?»
Оскільки Ar(C) < Ar(Ca), то Mr(CO) < Mr(CaO). Масова частка є відношенням відносної атомної маси Оксигену до відносної молекулярної маси речовини. Із двох дробів з однаковим чисельником більший є той, в якого менший знаменник, тому
w(CO) > w(CaO).
Відповідь: масова частка Оксигену більша в карбон (II) оксиді.
Завдання 6
Кава, шоколад і більшість енергетичних напоїв містять кофеїн, молекула якого складається з 8 атомів Карбону, 10 атомів Гідрогену, 4 атомів Нітрогену, 2 атомів Оксигену. Ця речовина дає змогу людині почуватися бадьорою та зосередженою, стимулює діяльність мозку. Однак, надмірне споживання кофеїну може спричинити безсоння, знервованість і підвищене серцебиття Також регулярне вживання кофеїну спричинює «звикання».
1. Чому кофеїн варто вживати в помірних кількостях. Щоб не спричинити безсоння, знервованість і підвищене серцебиття.
2. Визнач масові частки хімічних елементів у кофеїні.
Відомо: сполука C8H10N4O2
Знайти: w(C) – ?, w(H) – ?, w(N) – ?, w(O) – ?
Розв'язання
1. Обчислюємо відносну молекулярну масу сполуки.
Mr(C8H10N4O2) = 8Ar(C) + 10Ar(H) + 4Ar(N) + 2Ar(O) = 96 + 10 + 56 + 32 = 194
2. Обчислюємо масові частки елементів.
w(C) = 8Ar(C) : Mr(C8H10N4O2) = 96 : 194 = 0,495, або 49,5%
w(H) = 10Ar(H) : Mr(C8H10N4O2) = 10 : 194 = 0,051, або 5,1%
w(N) = 4Ar(N) : Mr(C8H10N4O2) = 56 : 194 = 0,289, або 28,9%
w(O) = 2Ar(O) : Mr(C8H10N4O2) = 32 : 194 = 0,165, або 16,5%
Відповідь: w(C) = 49,5%, w(H) = 5,1%, w(N) = 28,9%, w(O) = 16,5%
3. Підготуй ТОП–3 цікавих з твоєї точки зору фактів про кофеїн, щоб виголосити їх у класі. Зазнач використані джерела інформації.