Пригадуємо й застосовуємо
• Оформи опис водню за пунктами:
1. Хімічна формула, якісний і кількісний склад.
Молекула Н2 складається з двох атомів Гідрогену.
2. Агрегатний стан, колір, смак.
Газ, без кольору і смаку.
3. Проста чи складна, органічна чи неорганічна речовина.
Проста неорганічна речовина.
4. Відносна молекулярна, молярна маси.
Mr(H2)=2Ar(H)= 2•1 = 2, M(H2) = 2 г/моль
5. Відносна густина за повітрям.
Dповітря(H2)=Mr(H2) : Mr(повітря) = 2 : 29 = 0,069, або 6,9%
Де більше молекул: у 160 г водню чи у 160 г кисню?
Оскільки Мr(H2)< Mr(O2), тому n(H2)>n(O2) й, відповідно, N(H2)>N(O2)
Отже, більше молекул у 160 г водню.
• Що означають поняття «невідновлювані джерела енергії» і «відновлювані джерела енергії»? Наведи приклади.
Невідновлювані джерела енергії — це природні запаси речовин або енергії, які існують у обмеженій кількості, не поповнюються в масштабах людського життя і неминуче вичерпуються через використання людиною.
Приклади: вугілля, нафта, природний газ.
Відновлювані джерела енергії — це природні джерела, які постійно поповнюються в природі та є практично невичерпними в масштабах людського життя.
Приклад: сонячна енергія, вітрова енергія, гідроенергія, геотермальна енергія, біомаса.
ОПРАЦЮЙ ЗРОЗУМІЙ ВИКОРИСТАЙ
Завдання 1
Які підстави для визнання Гідрогену найпоширенішим елементом у Всесвіті?
Гідроген визнано найпоширенішим елементом у Всесвіті, оскільки він становить близько 90% за кількістю атомів. Він є основним компонентом зірок (у тому числі Сонця), міжзоряного газу та газових планет-гігантів.
Завдання 2
Побудуй діаграму масового вмісту Гідрогену в природних тілах.
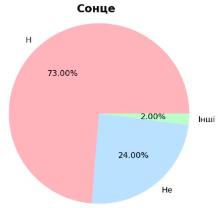 |
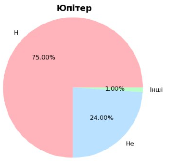 |
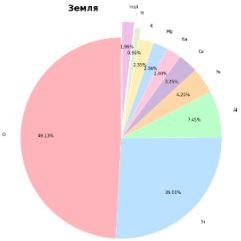 |
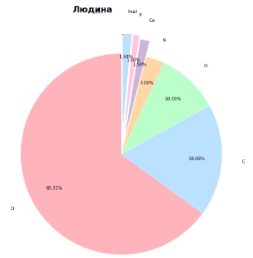 |
Завдання 3
Проаналізуй розглянуте рівняння і встанови / поясни, скільки реактантів і скільки продуктів у цій реакції; до простих чи складних речовин вони належать.
Zn + 2HCl = ZnCl2 + Н2↑
Реактанти два: Zn — проста речовина і HCl — складна речовина.
Продукти реакції два: ZnCl2 — складна речовина і Н2 — проста речовина.
Чи належить ця реакція до реакцій сполучення або розкладу?
Ця реакція не належить до реакцій сполучення або розкладу.
Завдання 4
Відшукай у тексті параграфа пояснення, чому водень є ефективним й екологічно безпечним паливом.
Водень — екологічно чисте паливо, тому що продуктом його горіння є вода.
Завдання 5
Склади рівняння змодельованої реакції. 2H2O = 2H2↑ + O2↑
|
Модель схеми реакції добування водню з води: |
||||
 |
електричний струм ------------------------> |
 |
+ |  |
 |
 |
|||
НУМО ДОСЛІДЖУВАТИ
ОДЕРЖАННЯ І ЗБИРАННЯ ВОДНЮ
Мета дослідження: навчитися одержувати і збирати водень у лабораторних умовах.
Обладнання і речовини: штатив лабораторний, прилад для добування газів, пробірки, штатив для пробірок, сірники, скіпка, гранули цинку Zn, розбавлена хлоридна кислота HCl.
Крок 1
Поясни, чому для збирання водню витісненням повітря пробірку необхідно розташовувати догори дном.
Водень легший за повітря, тому для збирання водню витісненням повітря пробірку необхідно розташовувати догори дном.
Крок 2
Запиши рівняння реакцій, які в ньому продемонстровано.
Zn + 2HCl = ZnCl2 + H2↑
Fe + 2HCl = FeCl2 + H2↑
Висновок. Водень одержано взаємодією активних металів з кислотою. Для його збирання використано метод витісненням води, бо водень дуже погано розчиняється у воді.
ТОБІ ДО СНАГИ
Вправа 1
Доведи або спростуй твердження: «Гідроген — найпоширеніший хімічний елемент у Всесвіті».
Атоми Гідрогену становлять 92 % атомів у Всесвіті. Водень — основний компонент зір і міжзоряного простору, міститься в космічних туманностях, трапляється на деяких планетах Сонячної системи.
Вправа 2
Запиши формули речовин у послідовності зменшення масової частки Гідрогену: СН4, С6Н12О6, NH3.
w1(H)=4Ar(H): Mr(CH4) = 4 : 16 = 0,25
w2(H)=12Ar(H): Mr(C6H12O6) = 12 : 180 = 0,07
w3(H)=3Ar(H): Mr(NH3) = 3 : 17 = 0,18
0,25 > 0,18 > 0,07
Відповідь: СН4, NH3, C6H12O6.
Вправа 3
Вибери малюнки правильного способу добування та збирання водню. Обґрунтуй свій вибір.
Мал. а) водень легший від повітря, тому, збираючи сетодом витісненням повітря, пробірку треба тримати отвором донизу.
Мал. б) водень погано розчиняється у воді, тому його можна зібрати способом витісненням води.
Вправа 4
Водень — легкий горючий газ. Як перевірити це твердження?
До отвору пробірки з воднем, зібраним методом витісненням повітря (водень легший за повітря), піднести запалений сірник. Водень загоряється з чутним звуком слабкого вибуху.
Вправа 5
Які об’єми водню і кисню (н. у.) взаємодіють з утворенням води масою 27 г?
Відомо: m(H2O) = 27 г
Знайти: V(H2) – ?, V(O2) – ?
Розв’язання
M(H2O)=18 г/моль
n(H2O) = m(H2O) : M(H2O) = 27 г : 18 г/моль = 1,5 моль
Записуємо рівняння реакції: 2H2 + O2 = 2H2O
n(H2):n(H2O)=2:2=1:1, звідси n(H2) = n(H2O) = 1,5 моль
n(О2):n(H2O) = 1 : 2, звідси n(O2) = n(H2O) : 2 = 1,5 моль : 2 = 0,75 моль
Обчислюємо об'єм кисню і водню.
V(H2) = n(H2) • Vm = 1,5 моль • 22,4 л/моль = 33,6 л
V(О2) = n(О2) • Vm = 0,75 моль • 22,4 л/моль = 16,8 л
Відповідь: 33,6 л Н2 і 16,8 л О2.
Вправа 6
Запиши хімічне рівняння взаємодії заліза із хлоридною кислотою, якщо один із продуктів реакції — ферум (ІІ) хлорид. Скориставшись записаним рівнянням, склади умову задачі на обчислення з використанням кількісних співвідношень речовин у цій хімічній реакції та розв’яжи задачу.
Який об’єм водню (н.у.) виділиться під час взаємодії заліза із хлоридної кислотою (н.у.), якщо утворився ферум (ІІ) хлорид кількістю речовини 2 моль?
Відомо: n(FeCl2) = 2 моль
Знайти: V(H2) – ?
Розв’язання
Записуємо рівняння реакції: Fe + 2HCl = FeCl2 + H2↑
n(FeCl2):n(H2)=1:1, звідси n(H2) = n(FeCl2) = 2 моль
Обчислюємо об'єм водню.
V(H2) = n(H2) • Vm = 2 моль • 22,4 л/моль = 44,8 л
Відповідь: 44,8 Н2.
Вправа 7
Близько ста років тому водень використовували для наповнення повітряних куль. Однак сучасні повітряні кулі наповнюють іншим газом — гелієм. На якій властивості водню ґрунтувалося його використання в наведеному прикладі? Які ризики, пов’язані з використанням водню для повітряних мандрівок, спонукали до його заміни гелієм?
Використання водню для наповнення повітряних куль ґрунтувалося на фізичній властивості: малій густині (легкий газ). Водень — горючий газ, його суміші з повітрям вибухають, а суміш водню з киснем у пропорції 2:1 називають «гримучим газом». Після трагедії великого дирижабля «Гінденбург» водень в повітроплаванні замінили гелієм.
Вправа 8
Схарактеризуй фізичні та хімічні властивості водню, які роблять його перспективним паливом. Чому водень вважається екологічно чистим джерелом енергії?
Рідкий водень використовується як вид ракетного палива, а стиснений — як паливо для двигунів автомобілів.
Водень горить з утворенням великої температури полум'я, тому реакцію горіння водню в чистому кисні застосовують для різання і зварювання металів, у двигунах космічних кораблів.
У металургії водень застосовують для відновлення з руд цінних металів, у харчовій промисловості — для перетворення рідких рослинних олій на тверді жири (маргарин).
Водень вважаєтьс екологічно чистим паливом, тому що продуктом його горіння є вода.