© 8next.com (відповіді, перероблене і доповнене)
Вправа 1
Склади графічну електронну формулу атома Флуору.
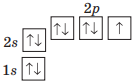
Скільки в ній:
а) спарених електронів; 8 електронів, або 4 пари електронів
б) неспарених електронів; 1 неспарений електрон
в) s–електронів; 4 електронів
г) р–електронів; 5 електронів
д) електронів не вистачає для завершення зовнішнього енергетичного рівня? 1 електрон
Вправа 2
Напиши графічні електронні формули Нітрогену й Флуору; зазнач, атом якого елемента має більше неспарених електронів.
| Нітроген | Флуор |
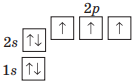 |
 |
Атом Нітрогену має більше неспарених електронів, бо в нього 3 неспарених електрони, а в атома Флуору — 1 неспарений електрон.
Вправа 3
Спрогнозуй вид хімічного зв’язку між атомами з такими електронними конфігураціями зовнішнього енергетичного рівня: …3s1 і …3s23p4.
Вправа 4
Якими способами атоми можуть досягати завершеності зовнішнього енергетичного рівня?
Атоми можуть досягати завершеності зовнішнього енергетичного рівня (зазвичай 8 електронів, для 1–го періоду — 2) втратою чи прийманням електронів під час утворення йонного зв'язку чи утворюючи спільні електронні пари під час утворення ковалентному зв'язку, що забезпечує досягнення стабільної електронної конфігурації інертного елемента.
Вправа 5
Дай відповідь на запитання: «Чим атом Калію відрізняється від йону Калію?».
Атом калію є електронейтральним, а йон Калію має позитивний заряд (+1). Електронна оболонка атома Калію містить 4 енергетичні рівні, на яких міститься 19 електронів, а йон Калію — 3 енергетичні рівні, на яких міститься 18 електронів.
Вправа 6
За наведеною будовою визнач і назви частинки речовини:
а) +3, 2е; Катіон Літію Li+
б) +8, 2е, 6е; Аніон Оксигену O2–
в) +9, 2е, 8е; Аніон Флуору F–
г) +20, 2е, 8е, 8е, 2е. Атом Кальцію Са
Вправа 7
Змоделюй утворення хімічного зв’язку в молекулі карбон (IІ) оксиду.
Вивчається у старших класах.
Атом Карбону в цьому оксиді перебуває в основному стані (6С 1s22s22p2) і має одну вакантну р–орбіталь. У його молекулі є два зв’язки між атомами С та О, що утворюються за обмінним механізмом, і ще один зв’язок — за донорноакцепторним механізмом:
![]()
Вправа 8
З наведеного переліку формул випиши формули речовин з ковалентним неполярним зв’язком:
BaO, Br2, MgCl2, CH4, SO2, H2, H2Se, О2, РH3, Na2O, CaF2.
Вправа 9
Порівняй хімічний зв’язок у молекулах хлору і гідроген хлориду, кисню й азоту. Заповни в зошиті таблицю результатами порівняння.
| Формули речовин |
Результати порівняння хімічного зв'язку | |
| спільне | відмінне | |
| Cl2, HCl | ковалентний | неполярний і полярний |
| О2, N2 | ковалентний неполярний | кратність (подвійний і потрійний) |
Вправа 10
Змоделюй утворення хімічного зв’язку в молекулі кисню, зазнач вид хімічного зв’язку, валентність і ступінь окиснення Оксигену в ній.
![]()
У молекулі кисню існує ковалентний неполярний зв'язок.
У молекулі кисню Оксиген має валентність (II) і ступінь окиснення 0.
Вправа 11
Запиши будову електронних оболонок катіона Кальцію та аніона Сульфуру і порівняй їх.
| Катіон Кальцію | Аніон Сульфура |
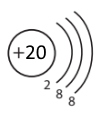 |
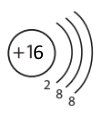 |
Електронна оболонка катіона Кальцію та аніона Сульфуру однакова: 3 енергетичні рівні, зовнішній енергетичний рівень завершений (8 електронів).
Вправа 12
Назви структурні частинки речовин, формули яких:
а) Н2О; молекули
б) О2; молекули
в) СаF2; йони
г) С (алмаз). атоми
Вправа 13
Склади схеми будови йонів K+, Mg2+, Cl–.
| Катіон Калію K+ | Катіон Магнію Mg2+ | Аніон Хлору Cl– |
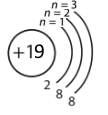 |
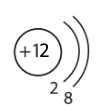 |
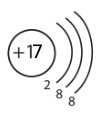 |
Формули утворених цими йонами бінарних сполук: KCl, MgCl2
Вправа 14
Назви частинки, що складаються з:
а) 15 протонів і 15 електронів; Атом Фосфору Р
б) 8 протонів і 10 електронів. Аніон Оксигену О2–
Вправа 15
Запиши формули речовин і класифікуй їх за різновидом хімічного зв’язку:
магній оксид MgO, чадний газ CO, азот N2, барій хлорид BaCl, вода H2O, кисень O2.
Класифікація речовин за різновидом хімічного зв'язку:
MgO, BaCl — йонний хімічний зв'язок,
N2,O2 — ковалентний неполярний зв'язок,
СO, Н2О — ковалентний полярний зв'язок.
Вправа 16
Яка відмінність між властивостями кристалічних речовин атомної, молекулярної та йонної будови? Наведи приклади.
Речовини молекулярної будови мають невелику твердість, легкоплавкі, леткі, часто мають запах, розчини проводять струм, більшість розчинні.
Приклади молекулярних речовин: йод, нафталін, сахароза, глюкоза.
Речовини атомної будови тверді, тугоплавкі, нелеткі, не проводять електричний струм, не розчиняються в жодних розчинниках.
Приклади атомних речовин: алмаз, силіцій (IV) карбід, силіцій(IV) оксид, графіт.
Речовини йонної будови тверді, тугоплавкі, нелеткі, в твердому стані не проводять електричний струм, більшість розчиняються у воді.
Приклади йонних речовин: кальцій флуорид, натрій хлорид, натрій гідроксид, пірит.
Вправа 17
Закінчи речення.
Найбільша електронегативність у Флуора.
Елемент у вільному стані має ступінь окиснення 0.
Зовнішній енергетичний рівень вважається завершеним, якщо він містить 8 електронів.
Вправа 18
Укажи якомога більше ознак, що характеризують рядок формул: MgO, Al2O3, FeO, Li2O.
Бінарні сполуки, оксиди металічних елементів, йонні речовини, мають йонний хімічний зв'язок, мають йонну кристалічну гратку, мають спільні фізичні властивості: тверді, тугоплавкі, нелеткі, в твердому стані не проводять електричний струм, більшість розчиняються у воді.
Вправа 19
Напиши формулу сполуки Фосфору із Хлором, у якій Фосфор виявляє свій максимальний ступінь окиснення (V), а Хлор — мінімальний (I). PCl5
Вправа 20
Склади формули бінарних сполук.
In2O3, Rb2O, TiO2, La2O3, WO3, Tc2O7, AsH3, Ac2O3, СаН2
§4 Короткі історичні відомості про спроби класифікації хімічних елементів
Знаємо, розуміємо
1. Пригадайте та назвіть відомі вам класифікації в інших науках. Біологічна класифікаія рослин і тварин, класифікація організмів за типами живлення.
2. За якими ознаками елементи було поділено на металічні та неметалічні? Властивості простих речовин (зовнішній прояв іхніх фізичних властивостей).
У чому недосконалість цієї класифікації? Бо є елементи, які залежно від умов можуть проявляти і металічні, і неметалічні властивості. Наприклад, Йод належить до неметалічних елементів, хоча утворена ним проста речовина йод I2 має металічний блиск. Типовий неметалічний елемент Карбон утворює просту речовину графіт, яка, подібно до металів, добре
проводить електричний струм.
3. За якими ознаками укладено класифікації елементів на тріади, октави? На тріади: за хімічною подібністю властивостей елементів, за значенням відносних атомних мас. На октави: за значення відносних атомних мас і започатковано нумерацію елемента.
4. Назвіть природні родини хімічних елементів.
Родина лужних елементів (Літій, Натрій, Калій, Рубідій, Цезій).
Родина галогенів (Флуор, Хлор, Бром, Йод, Астат)
Родина інертних елементів (Гелій, Неон, Аргон, Криптон, Радон).
Що стало загальною класифікаційною ознакою для їх виділення? Подібність властивостей елементів та їхніх сполук.
Застосовуємо
Вправа 17. Випишіть у хронологічному порядку зазначену в параграфі інформацію про кількість відомих у різні роки ХVIII–ХІХ століть хімічних елементів.
| Дата |
Кількість хімічних елементів |
|
1750 р. 1751–1800 рр. 1801–1850 рр. 1869 р. |
15 35 59 63 |
Вправа 18. Розробіть і самостійно заповніть таблицю «З історії класифікації хімічних елементів».
| Роки | Вчений |
Ознаки, які були використані для класифікації |
| 1786 – 1787 рр. | Антуан Лавуазьє | Властивості простих речовин |
| 1829 р. |
Йоганн Деберейнер |
Хімічна подібність елементів, значення відносних атомних мас |
| 1863 р. | Джон Ньюлендс |
Значення відносних атомних мас. Пронумерував елементи. |
| 1864 р. | Лотар Мейєр |
Значення відносних атомних мас, значення валентності. |