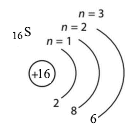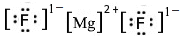Інші завдання дивись тут...
© 8next.com (відповіді, перероблене і доповнене)
• Поясни на прикладі конкретного металічного елемента, як змінюється будова електронної оболонки атома після втрати / віддачі електронів. Яка заряджена частинка утворюється при цьому?
Атом металічного елемента Натрій (Na), віддаючи 1 валентний електрон, набуває стійкої електронної оболонки атома інертного елемента Неон (Nе). При цьому атом перетворюється на позитивно заряджений йон — катіон Натрію (Na+).
• Поясни на прикладі конкретного неметалічного елемента, як змінюється будова електронної оболонки атома після приєднання / одержання електронів. На яку заряджену частинку перетворюється при цьому атом?
Атом неметалічного елемента Хлор (Cl), приєднуючи 1 валентний електрон, набуває стійкої електронної оболонки атома інертного елемента Аргон (Ar). При цьому атом перетворюється на негативно заряджений йон — аніон Хлору (Cl–).
• В яких агрегатних станах можуть перебувати речовини?
Речовини можуть перебувати в трьох агрегатних станах: твердому, рідкому і газоподібному.
ОПРАЦЮЙ ЗРОЗУМІЙ ВИКОРИСТАЙ
Завдання 1
До простих чи складних речовин належать речовини з йонним зв’язком? Відповідь обґрунтуй.
Речовини з йонним зв'язком належать до складних речовин, бо виникають між атомами металічного і неметалічного елементів, тобто між атомами різних хімічних елементів.
Завдання 2
Застосуй знання з фізики про електричний струм і поясни, чому йонні кристали за наявності заряджених частинок не проводять електричний струм.
Йонні кристали у твердому стані не проводять електричний струм, бо хоч мають заряджені частинки (йони), але вони не є вільними і не можуть переміщатися по всьому об'єму для створення напрямленого руху, адже міцно утримуються в вузлах кристалічної ґратки електростатичними силами.
ХІМІЧНА СКАРБНИЦЯ
До складу морської води входять різні солі. Із середнім вмістом деяких із них знайомить таблиця. За хімічними формулами наведених солей з’ясуй і запиши йони, з яких складаються кристалічні ґратки кожної солі, та співвідношення йонів у кристалі.
|
Сіль
|
Масова частка
у відсотках
|
Запис
йонів
|
Співвідношення
у йонному кристалі
|
| NaCl |
77,8 |
Na+ і Cl– |
1 : 1 |
| MgCl2 |
10,9 |
Mg2+ і Cl– |
1 : 2 |
| MgSO4 |
4,7 |
Mg2+ i SO42– |
1 : 1 |
| KCl |
2,5 |
K+ і Cl– |
1 : 1 |
| K2SO4 |
2,5 |
k+ i SO42– |
2 : 1 |
ТОБІ ДО СНАГИ
Вправа 1
Наведи свій приклад сполуки з йонним хімічним зв’язком і змоделюй його утворення.
Сполука з йонним зв'язком калій фторид KF.
Модель утворення йонного зв’язку між цими атомами:
Вправа 2
Заповни пропуски в реченні, використавши слова «більший», «менший»:
а) у катіона заряд ядра більший за заряд електронної оболонки;
б) в аніона заряд електронної оболонки менший за заряд ядра.
Вправа 3
Що спільного і чим відрізняються атом і катіон одного хімічного елемента? Наведи приклад.
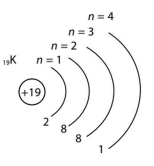
| Атом Калію (K) |
Катіон Калію (К+) |
 |
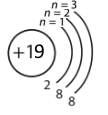 |
Для атома Калію і катіона Калію спільним є заряд ядра атома, що дорівнює +19.
Атом Калію і йон Калію відрізняються електронною оболонкою, а саме: кількістю енергетичних рівнів (4 і 3 відповідно), загальною кількістю електронів (19 і 18), кількістю електронів (1 і 8 відповідно) на зовнішньому енергетичному рівні.
Вправа 4
Що спільного і чим відрізняються атом та аніон одного хімічного елемента? Наведи приклад.
| Атом Сульфуру (S) |
Аніон Сульфуру (S–) |
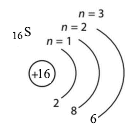 |
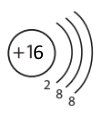
|
Для атома Сульфуру і аніона Сульфуру спільним є заряд ядра атома +16 та кількість енергетичних рівнів (3) в електронній оболонці.
Атом Сульфуру і аніон Сульфуру відрізняються кількістю електронів (16 і 18 відповідно), кількістю електронів на зовнішньому енергетичному рівні (6 і 8 відповідно).
Вправа 5
Класифікуй формули речовин за видом хімічного зв’язку: Na2O, OF2, Br2, HF, NH3, MgO, N2.
| Ковалентний зв'язок |
Йонний зв'язок |
| Полярний зв'язок |
Неполярний зв'язок |
Na2O, MgO
|
OF2, HF, NH3
|
Br2, N2
|
Ковалентний неполярний зв'язок виникає між атомами неметалічних елементів з однаковою електронегативністю, а полярний – з різною електронегативністю. Йонний зв'язок виникає між протилежно зарядженими йонами металічних і неметалічних елементів.
Вправа 6
Спрогнозуй вид хімічного зв’язку між атомами, що мають таку конфігурацію зовнішніх енергетичних рівнів: …3s2 і …2s22p5. Склади електронну формулу утвореної речовини.
В електронній оболонці атома на 3–ому енергетичному рівні 2 електрони, тому хімічний елемент міститься в 3 періоді і 2 групі періодичної таблиці — це хімічний елемент Магній (Mg). В електронній оболонці атома на 2–ому енергетичному рівні 7 електронів, тому хімічний елемент міститься в 2 періоді і 17 групі періодичної таблиці — це хімічний елемент Флуор (F). Між атомами металічного елемента Магній і неметалічного елемента Флуор виникає йонний хімічний зв'язок.
Електронна формула утвореної речовини.
Вправа 7
Укажи пару йонів, що мають однакову кількість електронів:
а) Ca2+ i S2–;
б) Mg2+ i Cl–.
Вправа 8
Атом хімічного елемента має на 2 електрони більше, ніж катіон Натрію. Установи назву елемента і наведи приклад його йонної сполуки.
Катіон Натрію містить 10 електронів, тому на 2 електрони більше: 10 + 2 = 12, отже, 12 електронів має атом хімічного елемента з порядковим номером 12 – це Магній (Mg).
Оскільки йонний зв'язок виникає між металічним елементом Магнієм і неметалічним елементом, наприклад, Хлором, тому приклад його йонної сполуки — це магній фторид MgF2.
___________ у виданні 2016 року______________
§20 Йони. Йонний зв'язок, його утворення
Знаємо, розуміємо
1. Сформулюйте визначення понять: катіон, аніон, іонний хімічний зв’язок.
Катіон – це позитивно заряджений йон.
Аніон – це негативно заряджений йон.
Йонний (іонний) хімічний зв’язок — це зв’язок між протилежно зарядженими йонами (катіонами й аніонами).
2. Порівняйте та розкажіть, що спільного й чим відрізняються:
а) атом і катіон одного хімічного елемента;
Спільне: будова ядра (протонне число, заряд ядра атома тощо).
Відмінне: будова електронної оболонки (у катіона менша кількість енергетичних рівнів, кількість електронів, ніж в атомі).
б) атом і аніон одного хімічного елемента?
Спільне: будова ядра (протонне число, заряд ядра атома тощо).
Відмінне: будова електронної оболонки (у аніона більша кількість електронів, ніж в атома).
Наведіть приклади.
|
Na0 +11 ))) – 1 e = Na+ +11 ))
281 28
атом Натрію йон (катіон) Натрію
|
|
Cl0 +17 ))) + 1 e = Cl– +17 )))
287 288
атом Хлору йон (аніон) Хлору
|
3. У чому полягає відмінність між ковалентним і йонним хімічними зв’язками?
Йонний зв'язок за механізмом утворення подібний до ковалентного, але має принципову відмінність: у речовинах з йонним зв'язком атоми жорстко не з'єднуються один з одним, а просто притягуються один до одного електростатистичними взаємодіями.
Вправа 61. Класифікуйте формули речовин за видом хімічних зв’язків на групи з ковалентним неполярним, ковалентним полярним, іонним зв’язками: PF3, CuO, OF2, Br2, MgS, HF, NH3.
|
Ковалентний
неполярний
|
Ковалентний
полярний
|
Іонний
|
| Br2 |
PF3, OF2,HF, NH3 |
CuO, MgS |
Вправа 62. Спрогнозуйте вид хімічного зв’язку між атомами, що мають таку будову зовнішніх енергетичних рівнів: …3s2 і …2s22p5. Напишіть формулу утвореної речовини.
Для …3s2: на третьому енергетичному рівні містяться 2 s–електрони, тому хімічний елемент розміщується у 3 періоді 2 групі головній підгрупі – це металічний елемент Магній.
Для …2s22p5: на другому енергетичному рівні містяться 7 електронів (2 s–електрони і 5 р–електронів), тому хімічний елемент розміщується у 2 періоді 7 групі головній підгрупі – це неметалічний елемент Флуор.
Формула MgF2. Між протилежно зарядженими йонами Магнію і Флуору виникає йонний зв'язок.
Вправа 63. Атом хімічного елемента має на 2 електрони більше, ніж катіон Натрію. Назвіть елемент.
Атом Натрію, віддаючи 1 електрон, перетворюється на катіон Натрію, що має 10 електронів. Тому атом невідомого елемента матиме 12 електронів (10+2=12), а на число електронів вказує порядковий номер елемента, тому невідомий хімічний елемент з порядковим №12 – це Магній.
Вправа 64. Атом хімічного елемента має на 3 електрони менше, ніж аніон Хлору. Назвіть елемент.
Атом Хлору, приєднуючи 1 електрон, перетворюється на аніон Хлору, що має 18 електронів. Тому атом невідомого елемента матиме 15 електронів (18–3=15), а на число електронів вказує порядковий номер елемента, тому невідомий хімічний елемент з порядковим №15 – це Фосфор.
Інші завдання дивись тут...