Інші завдання дивись тут...
© 8next.com (відповіді, перероблене і доповнене)
• Пригадай, що називають валентністю та як її позначають.
Валентність — це здатність атома зв’язуватися з певною кількістю інших атомів.
Валентність елементів має цілочисельні значення, її позначають римськими числами від І до VIII.
• Формули фосфор (V) оксиду P2O5, карбон (ІІ) оксиду CO2, сульфур (VІ) фториду SF6.
• Який вид хімічного зв’язку в цих сполуках? У цих сполуках ковалентний полярний зв'язок.
• Як він утворився? Ковалентний полярний зв’язок в цих сполуках утворився за допомогою спільних електронних пар, які зміщені до більш електронегативного атома, а саме до Оксигену і Флуору.
• Що означають записи Са2+, Сl–?
Запис Са2+ означає катіон Кальцію із зарядом +2, а Сl– — аніон Кальцію із зарядом –1.
ОПРАЦЮЙ ЗРОЗУМІЙ ВИКОРИСТАЙ
Завдання 1
Змоделюй утворення хімічних зв’язків у молекулах водню, азоту, кисню, метану. За кількістю хімічних зв’язків визнач валентність кожного атома у складених формулах.
| Речовини |
Водень |
Азот |
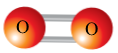
Кисень |
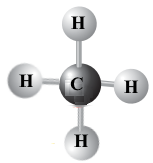
Метан |
|
Хімічні
формули
|
H2 |
N2 |
O2 |
CH4 |
|
Модель
молекули
|
 |
 |
 |
 |
|
Валентність
|
Гідрогену I
|
Нітрогену III
|
Оксигену II
|
Гідрогену I,
Карбону IV.
|
Завдання 2
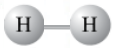
Визнач кількість спільних електронних пар у молекулі у молекулі гідроген сульфіду Н2S.
у молекулі гідроген сульфіду Н2S дві спільні електронні пари.
До якого атома вони зміщені?
Спільні електронні пари зміщені до більш електронегативного атома Сульфура S.
Які ступені окиснення елементів у цій сполуці?
За кількістю зміщених електронних пар встановлюємо, що ступінь окиснення Сульфуру дорівнює –2, а Гідрогену — +1.
Завдання 3
Поясни, чому в наведених прикладах атоми мають однаковий ступінь окиснення і різну валентність.
У простих речовинах неметалах N2, F2, O2 існує ковалентний неполярний зв'язок, спільна електронна пара не зсувається до жодного з атомів, тому ступінь окиснення елементів в простих речовинах завжди дорівнює нулю. Але атоми один з одним в молекулах зв'язані хімічним зв'язком, тобто виявляють певну валентність. В азоті N2 зв'язані потрійним зв'язком, тому виявляють валентність III, у фторі F2 — одинарним зв'язком, тому виявляють валентність I, а в кисні O2 — подвійним зв'язком, тому виявляють валентність II.
Визначили ступені окиснення Нітрогену у формулах: N2, N2O, N2O3, Li3N, NO2, NH3, Mg3N2.
N20, N2+4O, N2+3O3, Li3N-3, N+4O2, N+3H3, Mg3N2-3.
ПЛІЧ–О–ПЛІЧ
Cl2O, CCl4, Cl2O3, Cl2O5, HCl, Cl2O7, AlCl3.
Завдання 2
Чи з усіма відповіддями погоджуєтесь?
Якщо маєте власну думку, то озвучте її групі й аргументуйте.
1. Оксиген і Нітроген мають однаковий ступінь окиснення, але різну валентність.
Відповідь неправильна щодо всіх речовин, а правильна щодо простих речовин.
Оксиген і Нітроген можуть мати однаковий ступінь окиснення (0) у своїх простих речовинах О2 та N2, при цьому їхня валентність відрізняється: Оксиген у молекулі О2 двовалентний, а Нітроген у молекулі N2 — тривалентний.
2. В оксидах CrO і CrO3 Хром має однаковий ступінь окиснення.
Відповідь неправильна. Хром у сполуці CrO має ступінь окиснення +2, а в сполуці CrO3 — +3.
3. Ступінь окиснення Карбону у вуглекислому газі дорівнює ступеню його окиснення у метані.
Це твердження неправильне. Ступінь окиснення Карбону у вуглекислому газі CO2 становить +4, тоді як у метані CH4 він дорівнює –4.
ТОБІ ДО СНАГИ
Вправа 1
Сформулюй визначення ступеня окиснення, поясни, чи тотожне воно з поняттям валентності.
Ступінь окиснення — це умовний заряд атома у речовині, обчислений на основі припущення, що спільні електронні пари зміщені до атома більш електронегативного елемента.
Поняття ступеня окиснення не тотожне з поняттям валентності, адже поняття валентності стосується речовин із ковалентним зв’язком, у молекулах яких атоми зв’язуються спільною електронною парою/парами, а у йонних сполуках зв’язок утворюється між йонами, тому для них валентність як фізична величина не має сенсу.
Вправа 2
Поясни на основі електронної теорії хімічного зв’язку, чому металічні хімічні елементи у сполуках мають позитивний ступінь окиснення.
Металічні елементи у сполуках мають позитивний ступінь окиснення, бо їх атоми мають великий радіус і невелику кількість валентних електронів, які легко віддають і перетворюються на позитивно заряджений йон, адже в йонних сполуках заряд йона збігається за величиною і зарядом зі ступенем окиснення.
Вправа 3
Який елемент у сполуці, формула якої SF6, має позитивний ступінь окиснення, а який — негативний? Аргументуй свою відповідь.
У сполуці, формула якої SF6, елемент Флуор F є більш електронегативним у порівнянні з Хлором Cl, а беручи до уваги те, що елемент із більшою електронегативністю має негативний ступінь окиснення, з меншою — позитивний, робимо висновок, що елемент S має позитивний ступінь окиснення, а F — негативний ступінь окиснення.
Вправа 4
Склади формули оксидів Мангану Mn зі ступенями окиснення +2, +4, +6, +7.
MnO, MnO2, MnO3, Mn2O7
Вправа 5
Чи може Флуор набувати позитивного ступеня окиснення, а Сульфур — негативного?
Флуор не може набувати позитивного ступеня окиснення через найвищу
електронегативність серед усіх хімічних елементів, тому завжди має ступінь окиснення
–1 або 0 у простій сполуці F2. Атом Сульфура може як віддавати електрони, так і
приєднувати їх, тому може набувати як позитивного, так і негативного ступеня
окиснення, найчастіше –2.
Вправа 6
Увідповідни (позначено однаковим кольором) формулу оксиду і ступінь окиснення елемента в ньому.
| Формула оксиду |
Ступінь окиснення |
|
1 Cr2O3
2 MnO2
3 V2O5
4 MgO
|
А +1
Б +2
В +3
Г +4
Д +5
|
Відповідь:
1—В, 2—Г, 3—Д, 4—Б
Вправа 7
Склади формули бінарних сполук Нітрогену з Натрієм, Магнієм, Алюмінієм, Калієм.
Na3N, Mg3N2, AlN, K3N
––––––––––––– ПРОГРАМА 2016 року –––––––
§21 Ступінь окиснення та його визначення за хімічною формулою
ПРАВИЛА ВИЗНАЧЕННЯ СТУПЕНЯ ОКИСНЕННЯ.
Ступінь окиснення елементів у простих речовинах дорівнює нулю.
Ступінь окиснення простого йона відповідає його заряду.
Ступінь окиснення Гідрогену у більшості сполук дорівнює +1, а в сполуках з металами (гідридах) дорівнює –1.
Ступінь окиснення Флуору у всіх сполуках дорівнює –1.
Ступінь окиснення Оксигену у всіх сполуках –2, крім O+2F2 , Н2+1О2–1.
Ступінь окиснення металів у сполуках завжди позитивний.
Найвищий ступінь окиснення відповідає номеру групи, до якої належить елемент, за винятком Флуору, Оксигену.
Більш електронегативний елемент завжди має негативний ступінь окиснення.
Мінімальний (негативний) ступінь окиснення неметалічного елемента дорівнює номеру групи, в якій він перебуває, мінус 8.
ВЛАСТИВІСТЬ ЕЛЕКТРОНЕЙТРАЛЬНОСТІ: алгебраїчна сума ступенів окиснення атомів у хімічній сполуці завжди дорівнює нулю, а у складному йоні – заряду йона.
Знаємо, розуміємо
1. Сформулюйте означення ступеня окиснення. Ступінь окиснення — це умовний заряд атома в сполуці, обчислений на основі припущення про те, що сполука складається тільки з іонів.
2. Який ступінь окиснення мають атоми в двохатомних молекулах простих речовин? Нуль. Поясніть чому. Ступінь окиснення вказує також на полярність хімічних зв’язків у речовині, а в двохатомних молекулах простих речовин хімічні зв'язки неполярні.
3. Наведіть приклади атомів із позитивним, негативним та нульовим значеннями ступеня окиснення.
Атоми металічних елементів (наприклад, Li+, К+, Са+2, Mg+2, Al+3 тощо) можуть тільки віддавати електрони, тому у сполуках виявляють позитивні ступені окиснення.
Атоми неметалічних елементів можуть приєднувати електрони і віддавати, тобто виявляти як негативний, так і позитивний ступені окиснення. Якщо елемент є більш електронегативним, то він виявляє негативний ступінь окиснення (наприклад, Н–, N–3, Cl–2), а якщо менш електронегативним – позитивний ступінь окиснення (наприклад, H+, N+5, Cl+7).
Атоми простих речовин мають ступінь окиснення 0.
4. Як визначити ступінь окиснення хімічного елемента за формулою бінарної сполуки? Користуючись правилами цього параграфа.
Застосовуємо
Вправа 65. Визначте ступені окиснення елементів у поданих сполуках формулами:
С+2О–2, С+4О2–2, Ba+2H2–, Cr+6O3–2, Cr+2O–2, Cr2+3O3–2.
Ступені окиснення визначають, використовуючи правила, подані вище.
Наприклад, визначимо ступінь окиснення Хрому у сполуці Cr2O3.
Ступінь окиснення О (–2). Позначимо ступінь окиснення Хрому у сполуці через х: Cr2хO3–2,
тоді за властивістю електронейтральності 2•х+3•(–2)=0, звідси х=3.
Наприклад, визначимо ступінь окиснення Хрому у сполуці CrO3.
Ступінь окиснення О (–2). Позначимо ступінь окиснення Хрому у сполуці через х: CrхO3–2,
тоді за властивістю електронейтральності 1•х+3•(–2)=0, звідси х=6.
Аналогічно визначаємо у решти сполуках.
Вправа 66. Випишіть елементи, що в поданих прикладах мають однакові ступені окиснення: H2+O–2, Ba+2O–2, H+Br–, Na2+O–2, Al2+3S3–2.
Елементи Н+ і Na+ (мають ступінь окиснення +1), O–2 i S–2 (мають ступінь окиснення –2).
Вправа 67. Користуючись рядом електронегативності та знаннями про будову електронної оболонки атомів і хімічний зв’язок, складіть формули бінарних сполук:
а) Алюмінію з Бромом; AlBr3
б) Гідрогену з Йодом. HI
Вправа 68. За формулами сполук визначте, у якій із них Нітроген має найнижчий, а у якій — найвищий ступінь окиснення: NO, N2О, NO2, N2, N2O5, N2O.
Визначимо ступені окиснення у поданих сполуках.
N+2O–2, N2+О–2, N+4O2–2, N20, N2+5O5–2, N2+1O–2.
Найнижчий ступінь окиснення Нітрогену 0 у сполуці N2, а найвищий – це +5 у сполуці N2O5.
Інші завдання дивись тут...