![]()
I-IІ рівні
Вправа 1 Складіть молекулярну та структурну формули бензену й поясніть, як утворюються хімічні зв'язки у молекулі. С6Н6
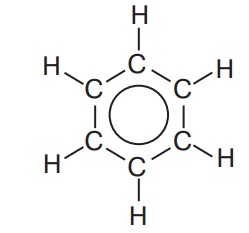
Кожний з атомів Карбону віддає по два електрони на утворення зв’язків між собою і один електрон — на утворення зв’язків з атомами Гідрогену. За рахунок четвертих електронів в молекулі бензену існує особливий вид хімічного зв’язку — ароматичний зв’язок. Під час його утворення одна р-орбіталь кожного атома Карбону перекривається з такими самими двома р-орбіталями (по одній від кожного сусіднього атома Карбону). Тому всі зв’язки С—С у бензені однакові й мають довжину 0,140 нм.
Вправа 2 Напишіть рівняння реакцій:
І варіант
а) 2C6H6 + 15O2 -> 12CO2 + 6H2O
б) C6H6 + 6Cl2 -> C6Cl6 + 6HCl (t,кат.)
II варіант
a)
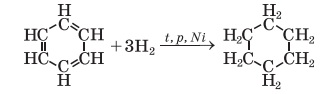
б) C6H6 + 3Cl2 -> C6H6Cl6 (за освітлення)
Вправа 3 Напишіть рівняння добування бензену способом ароматизації з:
а) гексану
С6Н14 -> C6H6 + 4H2
б) циклогексану
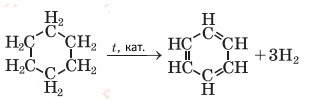
III рівень
Вправа 4 Поясніть, як практично довести, що під час горіння бензену утворюється вуглекислий газ і вода. Напишіть рівняння реакцій.
При пропусканні вуглекислого газу крізь розчин кальцій гідроксиду розчин стає каламутним.
Ca(OH)2 + CO2 = CaCO3↓ + H2O
Якщо над полум'ям потримати холодний предмет, то з часом помітимо на ньому краплі води.
Вправа 5 Напишіть рівняння реакцій за поданими схемами. Назвіть продукти реакцій та вкажіть умови перебігу.
І варіант
а ) С6H14 -> С6Н12 -> С6Н6 -> С6Н6Сl6
C6H14 -> C6H12 + H2 (кат., t0)

C6H6 + 3Cl2 -> C6H6Cl6
ІІ варіант
б) CaC2 -> C2H2 -> C6H6 -> C6H5Br
CaC2 + 2H2O -> Ca(OH)2 + C2H2
3C2H2 -> C6H6
C6H6 + Br2 -> C6H5Br + HBr (кат., t0)
Вправа 6 Розв'яжіть задачі.
І варіант
Задача 1 Бензен масою 32,5 кг з масовою часткою речовини 96% вступив у реакцію В з хлором в присутності каталізатора та за нагрівання. Обчисліть масу речовини, що утворилася та дайте їй назву.
Відомо: m(C6H6)=32,5 кг, ω(С6Н6)=96%
Знайти: m(С6H5Cl)-?
Розв'язування
mчистий(C6H6)=ω(С2H6)•m(C2H6):100%=96%•32,5 кг:100%=31,2 кг
Записуємо рівняння реакції:
31,2 кг х кг
C6H6 + Cl2 -> C6H5Cl + HCl
78 кг 112,5 кг
M(C6H6)=78 кг/кмоль, маса 1 кмоль=78 кг
M(C6H5Сl)=112,5 кг/кмоль, маса 1 кмоль=112,5 кг
х=m(C6H5Cl)=31,2 кг • 112,5 кг : 78 кг = 45 кг
Відповідь: 45 кг, хлоробензен
II варіант
Задача 2 Відносна густина парів арену за метаном - 4,875. Виведіть його молекулярну формулу, якщо загальна формула аренів - СnН2n-6. Дайте назву арену.
Відомо: СnН2n-6, DCH4(CnH2n-6)=4,875
Знайти: формулу СnН2n-6-?
Розв'язування
Mr(CnH2n-6)=DCH4(CnH2n-6)•Mr(CH4)=4,875•16=78
Mr(CnH2n-6)=n•Ar(C)+(2n-6)•Ar(H)=12n+2n-6=14n-6
Прирівняємо обидві частини, отримаємо алгебраїчне рівняння:
14n-6=78, звідси n=(78+6):14=6
Відповідь: С6Н6, бензен
Вправа 7 Напишіть рівняння реакцій між бензеном і запропонованими речовинами та укажіть умови їх перебігу:
I варіант
а) воднем;
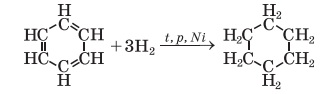
б) бромом за типом заміщення;
C6H6 + Br2 -> C6H5Br + HBr (t0, кат)
в) повного окиснення.
2C6H6 + 15O2 -> 12CO2 + 6H2O
II варіант
а) хлором за наявності каталізатора і нагрівання (2 випадки);
C6H6 + 6Cl2 -> C6Cl6 + 6HCl (t0, кат.)
C6H6 + Cl2 -> C6H5Cl + HCl (t0, AlCl3)
б) за сильного освітлення.
C6H6 + 3Cl2 -> C6Cl6 (hv)
Вправа 8 Розв'яжіть задачі.
І варіант
Задача 1 Масова частка Карбону у складі арену 92,31%. Густина пари речовини за гелієм 19,5. Виведіть молекулярну формулу сполуки. Напишіть її структурну формулу.
Відомо: СхНу, ω(С)=92,31%, або 0,9231, DНе(CxHy)=19,5
Знайти: формулу СхНу-?
Розв'язування
Mr(CxHy)=DНе(CxHy)•Mr(Не)=19,5•4=78
ω(Н)=1-ω(С)=1-0,9231=0,0769
х=ω(C)•Mr(CxHy):Ar(C)=0,9231•78:12=6
у=ω(Н)•Mr(CxHy):Ar(Н)=0,0769•78:1=6
Отже, формула сполуки С6Н6

II варіант
Задача 2 Бензен масою 34,2 г піддали дії хлору за нагрівання та присутності алюміній хлориду як каталізатора. Обчисліть маси та кількості речовин продуктів реакції.
Відомо: m(C6H6)=32,2 г
Знайти: m(С6H5Cl)-?
Розв'язування
Записуємо рівняння реакції:
34,2 г х г у г
C6H6 + Cl2 -> C6H5Cl + HCl
78 кг 112,5 г 36,6 г
M(C6H6)=78 г/моль, маса 1 моль=78 г
M(C6H5Сl)=112,5 г/моль, маса 1 моль=112,5 г
M(HCl)=36,5 г/моль, маса 1 моль=36,5 г
х=m(C6H5Cl)=34,2 г • 112,5 г : 78 г = 49,3 г
у=m(HCl)=34,2 г • 36,6 г : 78 г = 16 г
v(C6H5Cl)=m(C6H5Cl) : M(C6H5Cl)=49,3 г : 112,5 г/моль=0,44 моль
v(HCl)=m(HCl):M(HCl)=16 г : 36,5 г/моль=0,44 моль
Відповідь: 49,3 г і 0,44 моль С6H5Cl та 16 г і 0,44 моль HCl