Знаємо, розуміємо
Вправа 1. Назвіть характеристичну групу й наведіть приклади амінів.
Характеристична група амінів: аміногрупа NН2.
Приклади: метанамін CH3—NH2, етанамін CH3—СН2—NH2, феніламін (анілін) С6Н5—NН2
Вправа 2. Назвіть загальні формули амінів.
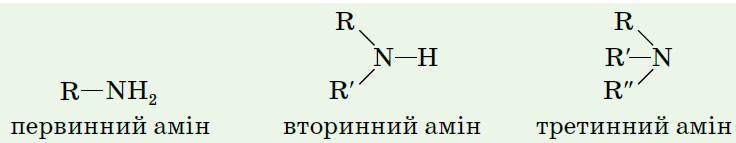
Вправа 3. Які класифікації амінів вам відомі? Що покладено в основу кожної з них? Залежно від замісника аміни бувають насиченими й ароматичними, а від кількості заміщених в амоніаці атомів Гідрогену — первинні, вторинні й третинні.
Вправа 4. Яка відмінність існує між первинними, вторинними, третинними насиченими й ароматичними амінами? Різною є природа вуглеводневих замісників (у насичених амінах залишок алкану, а в ароматичних - арену) і їхня кількість.
Вправа 5. Про які хімічні властивості метанаміну й аніліну ви дізнались?
Хімічні властивості метанаміну:
1. Горить з утворенням азоту, карбон (IV) оксиду та води:
4CH3NH2 + 9O2 -> 4CO2 + 10H2O + 2N2
2. Взаємодіє з водою:
СH3NH2 + H2O -> [CH3NH2]+ + OH- - метиламонію гідроксид
3. Взаємодіє з мінеральними кислотами:
СH3NH2 + HCl- → [CH3NH3]+Cl- - метиламонію хлорид
Хімічні властивості аніліну:
1. Взаємодіє з мінеральними кислотами:
С6Н5—NH2 + HCl → [C6H5—NH3]+ + Cl–
феніламоній хлорид
2. Взаємодіє з бромною водою:
С6Н5—NH2 + 3Br2 → C6H5—NH2Br3↓(білий осад) + 3HBr
2,4,6-триброманілін
Вправа 6. Як добувають анілін? У промисловості анілін добувають відновленням нітробензену С6Н5—NО2 за допомогою водню у присутності нікелевого чи мідного каталізаторів за нагрівання:
С6Н5—NО2 + 3Н2 -> С6Н5—NН2 + 2Н2О (каталізатор, t°С)
Де його використовують? У виробництві барвників, лікарських засобів.
Застосовуємо
Завдання 1. Складіть структурну формулу 3-етил-2,4-диметилгептан-1-аміну.
|
СH3—СH2—СH2—СH—СH—СH—СH2—NH2 │ │ │ СН3 С2Н5 СН3 |
Завдання 2. Установіть відповідність між формулою та речовиною.
| Формула | Речовина |
|
1 С6Н5OH 2 С6Н5NH2 3 С6Н6 4 С6Н5NO2 |
A нітробензен Б анілін В фенол Г бензен Д сорбіт |
Відповідь: 1-В, 2-Б, 3-Г, 4-А
Завдання 3. Складіть рівняння реакції етанаміну із хлоридною кислотою. Назвіть продукт реакції.
С2H5NH2 + HCl- → [C2H5NH3]+Cl- - етиламонію хлорид
Завдання 4. Обчисліть, яку масу аніліну можна одержати відновленням нітробензену кількістю речовини 4 моль.
Відомо: y(С6Н5—NО2)=4 моль
Знайти: m(С6Н5—NН2)-?
Розв'язування
І спосіб
С6Н5—NО2 + 3Н2 -> С6Н5—NН2 + 2Н2О
За рівнянням у(С6Н5—NО2):у(С6Н5—NН2)=1:1, кількості речовини однакові, тому
у(С6Н5—NН2)=у(С6Н5—NО2)=4 моль
M(С6Н5—NН2)=93 г/моль
m(С6Н5—NН2)=y(С6Н5—NН2)•М(С6Н5—NН2)=4 моль•93 г/моль=372 г
ІІ спосіб
4 моль х г
С6Н5—NО2 + 3Н2 -> С6Н5—NН2 + 2Н2О
1 моль 93 г
M(С6Н5—NН2)=93 г/моль, маса 1 моль=93 г
4 моль / 1 моль = х г / 93 г
х = 93 г • 4 моль : 1 моль=372 г
Відповідь: 372 г
Завдання 5. Обчисліть об’єм вуглекислого газу та азоту, що утворяться внаслідок спалювання етанаміну в кисні об’ємом 33,6 л (н.у.).
Відомо: V(O2)=33,6 л
Знайти: V(CO2)-?, V(N2)-?
Розв'язування:
4C2H5NH2 + 15O2 -> 8CO2 + 14H2O + 2N2
За рівнянням реакції V(O2):V(CO2)=15:8, тому
V(CO2)=8•V(O2):15=8•33,6:15=17,92 л
За рівнянням реакції V(O2):V(N2)=15:2, тому
V(N2)=2•V(O2):15=2•33,6:15=4,48 л
Відповідь: 17,92 л СО2 і 4,48 л N2