![]()
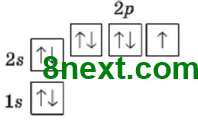
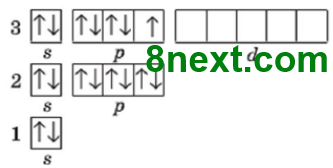
Вправа 1 Зобразіть графічні варіанти електронних формул Флуору та Хлору в основному стані й проаналізуйте їх.
|
9F0 1s22s22p5
|
|
17Cl0 1s22s22p63s23p5
|
Атоми якого із цих двох хімічних елементів можуть перейти в збуджений стан? Хлору
Чому? Бо в електронній оболонці атома Хлору, на відміну від Флуору, є вільні орбіталі
Вправа 2 Скількох електронів не вистачає атому кожного із цих елементів для набуття стійкої 8-електронної структури - октету? Одного електрона
Вправа 3 Якого ступеня окиснення набудуть Флуор та Хлор, якщо зовнішні енергетичні рівні їхніх атомів стануть завершеними? -1
Вправа 4 Скільки неспарених електронів в атомі Флуору й атомі Хлору в основному стані? Один
Вправа 5 Зобразіть графічні варіанти електронних формул атома Хлору в збудженому стані та проаналізуйте їх.
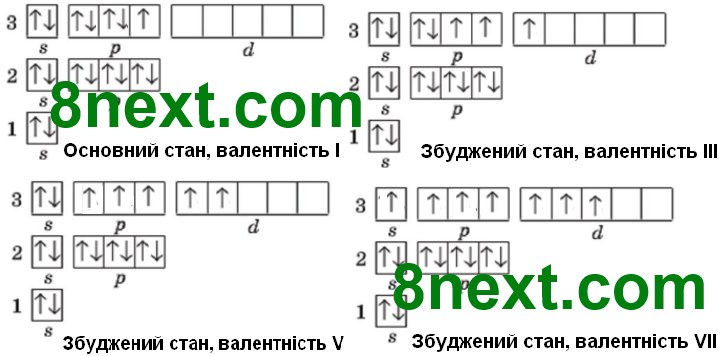 |
Вправа 6 Скільки неспарених електронів в атомі Хлору в першому збудженому стані? У другому? У третьому? У першому неспарених електронів три, у другому - п'ять, у третьому - сім
Скільки електронів може віддати атом Хлору в кожному із цих станів? Три, п'ять і сім
Якого ступеня окиснення набуде Хлор унаслідок цього? +3, +5, +7
Вправа 7 Складіть хімічні формули фторидів Хлору для основного та першого й другого збуджених станів атома Хлору. ClF, СlF3, ClF5
Вправа 8 Визначте ступені окиснення Хлору в речовинах:
СаСl2-1, Сl2+1O , NaCl-1O, КСl+5O3, NaCl+3O2, КСl+7O4, Сl20