САМОСТІЙНА РОБОТА (ФРОНТАЛЬНА)
Завдання 1. Нарисуйте s- i p- орбіталі та розташування р-орбіталей у просторі.
Які форми мають s- і р- орбіталі? S-орбіталь має форму кулі (сферичну), р-орбіталь має форму об'ємної вісімки (гантелі, причому ядро атома міститься у місці звуження гантелі).
Розташування р-орбіталей у просторі: вздовж осей х, у, z, тому їх ще називають Рх-, Ру-, Рz-орбіталями.

САМОСТІЙНА РОБОТА
І рівень
Завдання 1. Позначте елемент 3 періоду, який на зовнішньому енергетичному рівні має чотири електрони:
А. С. Б. О. В. Si. Г. P.
Число електронів зовнішнього енергетичного рівня для елементів головних підгруп співпадає з номером групи.
Завдання 2. Позначте елемент 2 періоду головної підгрупи V групи:
А. V. Б. N. В. Р. Г.S.
Завдання 3. Позначте вищий оксид елемента 2 періоду:
A. CO2 Б. Р2О3. В. SiO2 Г.Р2О5.
Завдання 4. Позначте вищу валентність Алюмінію за Оксигеном:
А. 4. Б. 5. В. 8. Г. 3.
Вища валентність дорівнює номеру групи, в якій розміщений елемент.
Завдання 5. Позначте формулу леткої сполуки неметалічного елемента з Гідрогеном 3 періоду:
А. СН4. Б. NH3. В. РН3. Г.Н2О.
Фосфор Р є елементом 3 періоду.
Завдання 6. Укажіть максимальне число електронів на 2р-підрівні:
А. 2. Б. 12. В. 8. Г. 6.
II рівень
Завдання 7. Позначте елемент, що має завершений енергетичний рівень:
А. Аr. Б. Аg. В. Аu. Г. As.
Інертні елементи мають завершений енергетичний рівень.
Завдання 8. Позначте два ВИЩИХ ОКСИДИ 2 і 3 періодів:
А. СО2. Б. Р2О3. В. SO3 Г. N2О.
Завдання 9. Позначте формулу леткої сполуки неметалічного елемента з Гідрогеном 2 періоду:
А. СН4. Б. РН3. В. НСІ. H2S.
Карбон С є елементом 2 періоду.
Завдання 10. Позначте максимальне число електронів на одній s-орбіталі:
А. лише 1. Б. 2 з антипаралельними спінами. В. 8.
III рівень
Завдання 11. Позначте назву орбіталі гантелеподібної форми:
А. s-орбіталь. Б.р-орбіталь. В. d-орбіталь. Г.f-орбіталь.
Завдання 12. Укажіть відповідність між елементом, номером періоду та номером групи:
| А. Не. | 1. 2. | I. VII. |
| Б. Мg. | 2. 1. | II. VIII. |
| B. F. | 3. 3. | III. II. |
Відповідь:
| А. |
2. | ІІ. |
| Б. |
3. | ІІІ. |
| В. | 1. | І. |
IV рівень
Завдання 13. Укажіть відповідність між елементом, номером періоду та електронною формулою:
| A. С. | 1. 4. | І. 1s22s22p63s23p1. |
| Б. Аl. | 2. 2. | II. 1s22s22p63s23p64s2. |
| B. Ca. | 3. 3. | III. 1s22s22p2 |
Відповідь:
| А. | 2. | ІІІ. |
| Б. |
3. | І. |
| В. |
1. | ІІ. |
Завдання 14. Напишіть формули вищих оксидів і гідратів оксидів елементів, поданих у завданні 13.
|
Символ елемента |
Вищий оксид
|
Гідрати оксидів |
|
С Al Ca |
СО2 Al2O3 CaO |
Н2СО3 Al(OH)3 Ca(OH)2 |
Обчисліть масову частку Алюмінію в алюміній гідроксиді.
Mr(Al(OH)3)=Ar(Al)+3•Ar(O)+3•Ar(H)=27+3•16+3•1=78
w(Al)=Ar(Al)/Mr(Al(OH)3)=27 / 78 = 0,346 або,
помноживши це число на 100%, одержимо 34,6%
Відповідь: w(Al)=0,346 або 34,6%
ДОМАШНЄ ЗАВДАННЯ
Вправа 1. Заповніть таблицю відповідними формулами.
|
№ елемента |
Хімічний символ |
Формула простої речовини |
Формула вищого оксиду |
Формула гідрату оксиду |
Формула леткої сполуки |
Характер оксиду та гідроксиду |
| 3 | Li | Li | Li2O | LiOH | - | основний |
| 7 | N | N2 | N2O5 | HNO3 | NH3 | кислотний |
| 12 | Mg | Mg | MgO | Mg(OH)2 | - | основний |
| 15 | P | P | P2O5 | H3PO4 | PH3 | кислотний |
Леткі сполуки з Гідрогеном утворюють тільки неметалічні елементи.
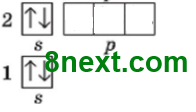
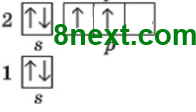
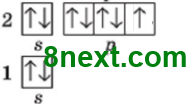
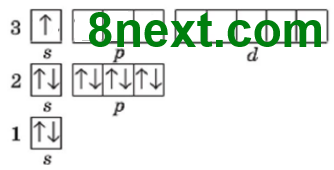
Вправа 2. Зобразіть будову електронних оболонок вказаних елементів електронними формулами й електронними графічними формулами і дані впишіть у таблицю.
|
№ еле- мен- та |
Електронна формула |
Графічна електронна формула |
Число елект- ронів на зов- нішньо- му рівні |
Бракує елект- ронів до за- вершен- ня рівня |
| 4 | 1s22s2 |
|
2 | 6 |
| 6 | 1s22s22p2 |
|
4 | 4 |
| 9 | 1s22s22p5 |
|
7 | 1 |
| 11 | 1s22s22p63s1 |
|
1 | 7 |
Завершеним рівнем вважається такий зовнішній енергетичний рівень, на якому міститься 8 електронів.
Вправа 3. Впишіть у вільні квадратики символи елементів 3 періоду, нарисуйте орбіталі s- і р-електронів та порядок їх заповнення, напишіть електронні формули. Порівняйте ваші результати з порядком заповнення зовнішнього енергетичного рівня для елементів 2 періоду. Зробіть висновки.
Заповнення комірок третього періоду аналогічне заповненому другому періоду (див. стор.29). Відмінності: у кожній комірці замість 2 пишете 3, бо є три енергетичні рівні, елементи другого періоду послідовно замініть елементами третього періоду: Li->Na, Be->Mg, B->Al, C->Si, N->P, O->S, F->Cl, Ne->Ar, решта все однакове.
ВИСНОВКИ. В елементів третього періоду з’являється додатковий третій енергетичний рівень, заповнення якого електронами аналогічне елементам другому періоду.
Вправа 4. Елементи А і Б знаходяться, відповідно, у І та VII групах періодичної системи Сполука АБ відома як харчовий продукт. Два інші - В і Г - елементи 2 періоду, які утворюють два оксиди. Перша сполука ВГ - отруйний газ, а друга - газ, що не підтримує горіння. Назвіть елементи А, Б, В, Г. Напишіть формули згаданих сполук і дайте їм назви.
|
А - Na (Натрій) Б - Cl (Хлор) АБ - NaCl (натрій хлорид)
|
В - C (Карбон) Г - О (Оксиген) ВГ - СО (чадний газ), СО2 (вуглекислий газ) |