![]()
Початковий рівень
Вправа 1 За якою формулою обчислюють кількість орбіталей на енергетичному рівні? За формулою n2, де n — номер рівня.
Вправа 2 Скільки орбіталей є на І енергетичному рівні? на ІІ? на ІІІ?
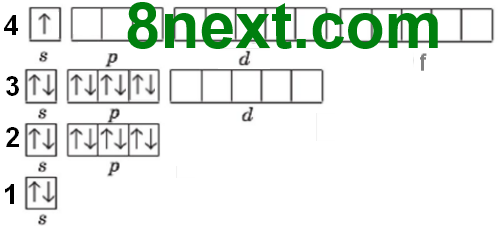
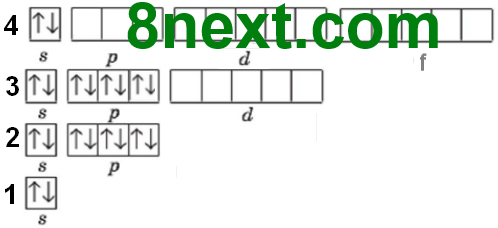
На першому енергетичному рівні є одна s-орбіталь (12=1),
на другому — одна s-орбіталь і три р-орбіталі, разом 4 орбіталі (22=4),
на третьому — одна s-орбіталь, три р-орбіталі і п’ять d-орбіталей, разом 9 орбіталей (32=9).
Вправа 3 Скільки енергетичних рівнів в атомі:
а) Гідрогену
Один енергетичний рівень
б) Натрію;
Три енергетичні рівні
в) Кальцію?
Чотири енергетичні рівні
Пояснення: кількість енергетичних рівнів в електронній оболонці атома елемента дорівнює номеру періоду, в якому цей елемент перебуває.
Середній рівень
Вправа 4 Енергія якого електрона — 1s чи 2s — є меншою?
Електрони першого рівня мають найменшу енергію, тобто енергія електрона 1s є меншою.
Вправа 5 Укажіть максимальну кількість електронів на 2s-підрівні:
А) 1
Б) 2
В) 6
Г) 10
Відповідь: Б
Пояснення: на 2s-підрівні міститься одна s-орбіталь на якій максимально може бути 2 електрони.
Вправа 6 Укажіть неправильне позначення:
А) 1s
Б) 1р
В) 2s
Г) 3р
Відповідь: Б
Достатній рівень
Вправа 7 Які електрони в атомі Сульфуру є зовнішніми?
Електрони третього енергетичного рівня, адже Сульфур перебуває в 3 періоді.
Вправа 8 Електрони якого рівня і підрівня в атомі Фосфору спарені?
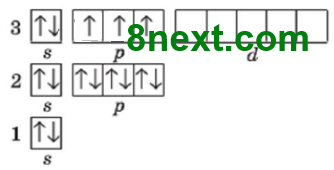
Відповідь: першого рівня і 1s-підрівня, другого рівня і 2s- та 2p-підрівнів, третього рівня і 3s-підрівня
Вправа 9 Електрон якого рівня і підрівня в атомі Хлору є неспареним?
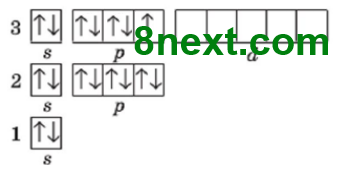
Відповідь: третього рівня і 3р-підрівня
Вправа 10 Складіть електронні графічні формули атомів Калію і Кальцію.
|
Графічна формула Калію:
|
|
Графічна формула Кальцію:
|
Високий рівень
Вправа 11 Установіть назву хімічного елемента, який утворює аніон Е- з електронною формулою зовнішнього електроного шару 3s23р6.
Електронна формула зовнішнього енергетичного рівня ...3s23p6. Заповнюється третій рівень, значить, елемент розташований у 3-му періоді. На зовнішньому рівні в нього 2+6=8 електронів, отже, елемент розташований у VІІІ групі. Це р-елемент. Шукаємо в Періодичній системі клітинку на перетині 3-го періоду й VІІІ групи. Цей елемент — Аргон.
Відповідь: Аргон
Вправа 12* Зовнішній електронний шар атома невідомого хімічного елемента має будову ns2np2. Молекулярна маса його леткої сполуки з Гідрогеном дорівнює молекулярній масі кисню. Установіть назву невідомого хімічного елемента.
Будову ns2np2 має атом невідомого елемента Е, на зовнішньому рівні в нього 2+2=4 електрони, отже, елемент розташовується в ІV групі головній підгрупі, тому формула його леткої сполуки з Гідрогеном має загальний вигляд ЕН4.
За умовою Mr(EH4)=Mr(O2)=32, тому Ar(E)+4•Ar(H)=32, звідси
Ar(E)=32-4•Ar(H)=32-4•1=28 Таку відносну атомну масу має атом елемента IV групи Силіцій Si
Відповідь: Силіцій