![]()
Контрольні запитання
Запитання 1
Дайте визначення поняттям «відносна атомна маса» і «відносна молекулярна маса».
Відносна атомна маса Ar — це відношення маси атома даного елемента до 1/12 маси атома Карбону. Відносна молекулярна маса Мr показує, у скільки разів маса молекули більша за 1/12 маси атома Карбону.
Що в даному випадку означає слово «відносна»?
Визначена порівнянням з іншою величиною — еталоном. Еталоном атомних і молекулярних мас є атомна одиниця маси (1а.о.м.=1,66•10-24г).
Запитання 2
Для яких речовин використовують термін «молекулярна маса», а для яких — «формульна маса»?
Для речовин молекулярної будови використовують термін «молекулярна маса», а для речовин немолекулярної (йонної та атомної) будови — «формульна маса».
Запитання 3
Як визначають відносну молекулярну масу?
Відносна молекулярна маса дорівнює сумі відносних атомних мас усіх хімічних елементів, що містяться у складі молекули, з урахуванням числа атомів кожного елемента.
Для визначення відносної молекулярної маси речовини з формулою EхDу необхідно відносні атомні маси елементів E та D помножити на число їхніх атомів, відповідно на х та у, а потім підсумувати: Mr(ExDy)=x●Ar(E)+y●Ar(D)
Запитання 4
Дайте визначення масової частки елемента в речовині та масової частки розчиненої речовини в розчині. Наведіть формули для їх обчислення.
Масова частка елемента показує, яка частина маси речовини припадає на атоми даного елемента.
Її обчислюють як відношення атомної маси даного елемента з урахуванням числа його атомів у молекулі до відносної молекулярної маси речовини:
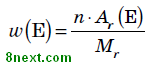
де ω(E) — масова частка хімічного елемента E, виражена в частках одиниці;
n — число атомів елемента E, позначене індексом у формулі сполуки;
Ar — відносна атомна маса елемента E;
Mr — відносна молекулярна маса речовини.
Масова частка розчиненої речовини в розчині показує, яка частина маси розчину припадає на розчинену речовину.
Масову частку розчиненої речовини обчислюють за формулою:
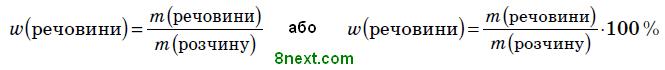
Завдання для засвоєння матеріалу
Вправа 1
Обчисліть відносні молекулярні (формульні) маси таких речовин: хлор Сl2, сульфатна кислота H2SO4, сахароза C12H22O11, гідроген пероксид (перекис водню) Н2O2, кальцій сульфат (гіпс) CaSO4, крейда СаСO3, малахіт (CuOH)2CO3.
Mr(Cl2)=2•Ar(Cl)=2•35,5=71
Mr(H2SO4)=2•Ar(H)+Ar(S)+4•Ar(O)=2•1+32+4•16=98
Mr(C12H22O11)=12•Ar(C)+22•Ar(H)+11•Ar(O)=12•12+22•1+11•16=342
Mr(H2O2)=2•Ar(H)+2•Ar(O)=2•1+2•16=34
Mr(CaSO4)=Ar(Ca)+Ar(S)+4•Ar(O)=40+32+4•16=136
Mr(CaCO3)=Ar(Ca)+Ar(C)+3•Ar(O)=40+12+3•16=100
Mr((CuOH)2CO3)=2•Ar(Cu)+2•Ar(H)+Ar(C)+5•Ar(O)=2•64+2•1+12+5•16=222
Вправа 2
Обчисліть масові частки всіх елементів у сполуках з такими хімічними формулами:
a) NO2
Mr(NO2)=Ar(N)+2•Ar(O)=14+2•16=46
ω(N)=Ar(N)/Mr(NO2)=14:46=0,304, або 30,4%
Масову частку Оксигену можна знайти так:
ω(О)=100%-ω(N)=100%-30,4%=69,6%
або так:
ω(О)=1-ω(N)=1-0,304=0,696
чи так:
ω(О)=2•Ar(О)/Mr(NO2)=2•16:46=0,696, або 69,6%
Відповідь: ω(N)=0,304, або 30,4%; ω(О)=0,696, або 69,6%
6) РbСl2
Mr(PbCl2)=Ar(Pb)+2•Ar(Cl)=207+2•35,5=278
ω(Pb)=Ar(Pb)/Mr(PbCl2)=207:278=0,745, або 74,5%
ω(Cl)=100%-ω(Pb)=100%-74,5%=25,5%
Відповідь: ω(Pb)=74,5%, ω(Cl)=25,5%
в) Na2CO3
Mr(Na2CO3)=2•Ar(Na)+Ar(C)+3•Ar(O)=2•23+12+3•16=106
ω(Na)=2•Ar(Na)/Mr(Na2CO3)=2•23:106=0,434, або 43,4%
ω(C)=Ar(C)/Mr(Na2CO3)=12:106=0,113, або 11,3%
ω(O)=100%-ω(Na)-ω(C)=100%-43,4%-11,3%=45,3%
Відповідь: ω(Na)=43,4%, ω(C)=11,3%, ω(O)=45,3%
г) H2SO4
Mr(H2SO4)=2•Ar(H)+Ar(S)+4•Ar(O)=2•1+32+4•16=98
ω(H)=2•Ar(H)/Mr(H2SO4)=2•1:98=0,02, або 2%
ω(S)=Ar(S)/Mr(H2SO4)=32:98=0,327, або 32,7%
ω(O)=100%-ω(H)-ω(S)=100%-2%-32,7%=65,3%
Відповідь: ω(H)=2%, ω(S)=32,7%, ω(O)=65,3%
д) Ва3(РO4)2
Mr(Ba3(PO4)2)=3•Ar(Ba)+2•Ar(P)+8•Ar(O)=3•137+2•31+8•16=601
ω(Ba)=3•Ar(Ba)/Mr(Ba3(PO4)2)=3•137:601=0,684, або 68,4%
ω(P)=2•Ar(P)/Mr(Ba2(PO4)2)=2•31:601=0,103, або 10,3%
ω(O)=100%-ω(Ba)-ω(P)=100%-68,4%-10,3%=21,3%
Відповідь: ω(Ba)=68,4%, ω(P)=10,3%, ω(O)=21,3%
---------------------------- ПРОГРАМА 2016 року ---------------------------------
Вправа 3 У розчині масою 120 г міститься глюкоза масою 3 г. Визначте масову частку розчиненої речовини.
Відомо: m(р-ну) = 120 г, m(глюкози)=3 г
Знайти: ω(глюкози)-?
І спосіб
ω(глюкози)=m(глюкози)/m(р-ну)=3 г:120 г=0,025, або 2,5%
ІІ спосіб
Для визначення масової частки глюкози складаємо пропорцію і розв'язуємо її:
в 120 г розчину міститься 3 г глюкози, а
в 100 г розчину ― х г глюкози
120 г / 100 г = 3 г / х г, звідси
х=3 г • 100 г : 120 г=2,5 г, тому ω(глюкози)=2,5%
Відповідь: ω(глюкози)=2,5%
Вправа 4. Обчисліть масу солі, що лишиться при випарюванні води з розчину масою 150 г, у якому масова частка солі становить 5%.
Дано: m(р-ну)=150 г, ω(солі)=5%
Знайти: m(солі)-?
І спосіб
m(солі)=ω(солі)•m(р-ну):100%=5%•150 г:100%=7,5 г
ІІ спосіб
Для визначення маси солі складаємо пропорцію і розв'язуємо її:
в 100 г розчину міститься 5 г солі, а
в 150 г розчину ― х г солі
100 г / 150 г = 5 г / х г, звідси
х=5 г • 150 г : 100 г=7,5 г
Відповідь: m(солі)=7,5 г