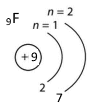Інші завдання дивись тут...
Сторінка 53
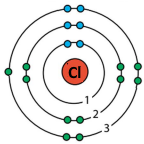
§25 Будова атома
Вправа 2
1. Атом — найменша хімічно неподільна частинка. +
2. Атом складається з ядра, навколо якого рухаються електрони. +
3. Ядро заряджене позитивно. +
4. Електрони заряджені негативно. +
5. Кількість позитивних і негативних зарядів в атомі однакова. +
6. Атом має позитивний заряд. –
7. В атомі містяться заряджені частинки. +
8. Електрон — центральна частина атома. –
9. Маса ядра вдвічі менша від маси атома. –
Вправа 3
Ядро — центральна частина атома, що складається з двох типів субатомних частинок протонів і нейтронів.
Субатомні частинки — протони, нейтрони, електрони.
Нуклон — загальна назва частинок, з яких складається ядро атома (протонів і нейтронів).
Протонне число — кількість протонів у ядрі атома елемента.
Масове число (нуклонне число) — загальна кількість нуклонів у ядрі атома елемента.
Нуклід — вид атома, що характеризується певним значенням протонного й масового числа.
Ізотопи — нукліди одного елемента з однаковим протонним числом, але різним масовим числом.
Таблиця 1
|
Назва хімічного
елемента
|
Символ
елемента
|
Протонне
число
|
Масове
число
|
| Нітроген |
N |
7 |
14 |
| Плюмбум |
Pb |
82 |
207 |
| Кальцій |
Са |
20 |
40 |
Таблиця 2
|
Нуклід
|
Порядковий номер
елемента
|
Кількість
протонів
|
Заряд
ядра
|
Кількість
електронів
|
Кількість
нейтронів
|
| 23Na |
11 |
11 |
+11 |
11 |
12 |
| 39К |
19 |
19 |
+19 |
19 |
20 |
| 55Mn |
25 |
25 |
+25 |
25 |
30 |
Вправа 4
Використовуючи додаткові джерела інформації, відшукайте, які нукліди Гідрогену, Карбону й Оксигену існують в природі.
Гідроген Н: 1Н (Протій), 2Н (Дейтерій), 3Н (Тритій).
Карбон С: 12С, 13С, 14С.
Оксиген О: 16О, 17О, 18О.
Сторінка 54
Заповніть таблицю.
|
Символ
елемента
|
Нуклід |
Порядковий
номер
|
Кількість
протонів
|
Заряд
ядра
|
Кількість
електронів
|
Кількість
нейтронів
|
| H |
1H |
1 |
1 |
+1 |
1 |
0 |
| C |
12C |
6 |
6 |
+6 |
6 |
6 |
| O |
16O |
8 |
8 |
+8 |
8 |
8 |
Розгадайте кросворд
Слово: ІЗОТОП
3 Літій
59 Празеодим
41 Ніобій
85 Астат
5 Бор
29 Купруп
З'єднайте позначення нуклідів із їх складом.
37Cl — 17 електронів, 20 нейтронів
12C — 6 електронів, 6 нейтронів
20 Ne — 10 електрони, 10 нейтронів
31P — 15 електронів, 16 нейтронів
40K — 19 електронів, 21 нейтрон
40Ca — 20 електронів, 20 нейтронів
35Cl — 17 електронів, 18 нейтронів
Вправа 5
Склали ментальну карту "Будова атома"
| ядро |
Будова атома |
електрони |
| протони |
електронна оболонка |
| нейтрони |
заряд атома |
Сторінка 55
§26 Електронна оболонка атома й властивості хімічних елементів
Вправа 2
Прочитайте твердження.
1. Нукліди 3517Cl і 3717Cl містять однакову кількість електронів. + Помилковий запис нуклідів
2. Заряд ядра атома Кальцію вдвічі більший за заряд ядра атома Натрію. –
3. Нукліди Карбон–12 і Оксиґен–16 є ізотопами. –
4. Ядро нукліда 115В містить 5 нейтронів. –
5. Протонне число атома Літію дорівнює масовому числу Тритію. +
6. Ядро нукліда 2412Mg містить однакові кількості протонів і нейтронів. +
7. Кількість електронів у нукліді Силіцій–28 дорівнює кількості нейтронів у ядрі нукліда 2713Al. –
8. Кількість протонів в ядрі атома Оксиґену вдвічі менша за кількість протонів в ядрі атома Сульфуру.+
9. Масове число нукліда 4020Cа дорівнює сумі протонних чисел атомів Флуору і Натрію.–
Вправа 3
Конспект до теми.
електронну оболону
рівнів
періоду
зовнішнім
Схеми будови електронних оболонок.
| Натрій Na |
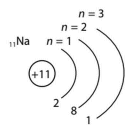 |
Флуор F |
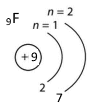 |
Елемент Натрій міститься в 1 групі, тому є металічним елементом, а Флуор — в VII, або 17 групі, тому є неметалічним елементом.
Розгляньте таблицю електронегативності (за Полінгом).
Електронегативність елементів у періоді посилюється зліва направо, а в групах послаблюється зверху вниз.
Запишіть назви і символи хімічних елементів із найменшим і найбільшим значенням електронегативності.
Цезій Cs (7.0) та Францій F (7.0) найменш електронегативні елементи, а Флуор (4.0) найбільш електронегативниий елемент.
Сторінка 56
Електронегативність яких елементів буде мати вищі значення — металічних чи неметалічних?
Атоми неметалічних елементів притягують електрони, тому будуть мати вищі значення електронегативності, ніж металічні.
Вправа 4
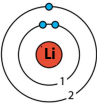
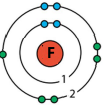
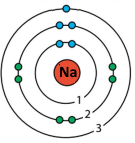
Моделі атомів 2–го і 3–го періодів періодичної таблиці.
Чи помітили ви якість закономірності? Складіть висновки.
За номером періоду можна визначити кількість енергетичних рівнів в електронній оболонці атома елемента.
За номером групи можна визначити кількість електронів на зовнішньому енергетичному рівні в атомі елемента.
Вправа 5
| 2ē, 5ē |
N |
2ē, 3ē |
B |
|
2ē, 8ē, 6ē |
S |
| 2ē, 8ē, 2ē |
Mg |
2ē, 1ē |
Li |
|
2ē, 8ē, 8ē |
Ar |
Сторінка 57
§27 Ступені окиснення хімічних елементів
Вправа 2
Складіть схему будови електронних оболонок атома Натрію та прочитайте твердження.
1. Порядковий номер цього елемента 11. +
2. Заряд ядра атома Натрію +3. –
3. Кількість протонів у ядрі атома Натрію – 10. –
4. Кількість електронів в атомі Натрію – 11. +
5. Кількість нейтронів у ядрі атома Натрію – 12. +
6. Зовнішній енергетичний рівень атома Натрію завершений. –
7. На зовнішньому енергетичному рівні атома Натрію міститься 3 електрони. –
8. За номером періоду можна визначити кількість енергетичних рівнів в електронній оболонці атома елемента. +
9. Кількість електронів на зовнішньому енергетичному рівні в атомі елемента визначають за порядковим номером. –
Вправа 3
Ступінь окиснення — це умовний заряд атома в разі припущення, що сполука складається лише з йонів.
Ступінь окиснення може мати додатні, від’ємні значення (а також нуль).
Ступінь окиснення змінюється в межах від –4 до +8.
Визначте заряд йонів у сполуках.
K+I–, Ba2+Cl2–, Ca32+N23–, Al23+S32–, K3+P3–, Na+F–, Mg2+O2–, Li+H–
Складіть формули і назвіть сполуки
| катіон |
аніон |
формула |
катіони |
аніони |
формула |
| Натрій Na+ |
фосфід F– |
NaF |
Кальцій Ca2+ |
карбід C4– |
CaC2 |
| Алюміній Al3+ |
карбід C4– |
Al4C3 |
Гідроген H+ |
оксид О2– |
H2O |
У порядку збільшення електронегативності:
1) Натрій, Магній, Силіцій, Фосфор, Сульфур, Хлор
2) Талій, Індій, Галій, Алюміній, Бор
Ступені окиснення у сполуках:
Mn2+7O7-2, N20, Na+1Br-1, Cr2-3S3+2, S80, S+6O3-2, O30, Li+1H-1
Cтупінь окиснення Хлору у сполуках:
Cl20, Ba+2Cl2-1, Cl2+1O-2
Складіть хімічні формули сполук
1 електрон і 6 протонів: CH4
14 протонів і 8 електронів: SiC
1 протон і 15 електронів: РН3
Сторінка 58
Обчисліть масові частки елементів із додатними ступенями окиснення.
Для сполуки СН4:
Mr(CH4)= Ar(C) + 4Ar(H) = 12 + 4 • 1 = 16
w(C) = Ar(C)/Mr(CH4) = 12 : 16 = 0,75, або 75%
Для сполуки SiC:
Mr(SiC)= Ar(Si) + Ar(C) = 28 + 12 = 40
w(Si) = Ar(Si)/Mr(SiС) = 28 : 40 = 0,7, або 70%
Для сполуки PH3:
Mr(PH3)= Ar(P) + 3Ar(H) = 31 + 3 • 1 = 34
w(P) = Ar(P)/Mr(PH3) = 31 : 34 = 0,92, або 92%
У розробці! Далі буде...
Інші завдання дивись тут...