Інші завдання дивись тут...
Сторінка 65
§30 Хімічний зв'язок. Різновиди хімічного зв'язку
Вправа 2
1. Заряд ядра атома чисельно дорівнює порядковому номеру елемента. +
2. Кількість енергетичних рівнів у атомі елемента дорівнює номеру групи Періодичної таблиці, в якій міститься цей елемент. –
3. Флуор у сполуках завжди проявляє ступінь окиснення –2. –
4. У періоді зліва направо металічні властивості посилюються. –
5. Катіони — це позитивно заряджені йони, які утворюються унаслідок втрати електронів. +
6. У групі зверху вниз радіус атомів зменшується. –
7. Атоми елементів однієї групи мають однакову кількість електронів на зовнішньому рівні. +
8. Номер періоду визначає кількість протонів у ядрі атома. –
9. Ступінь окиснення Оксигену у сполуці MgO дорівнює ступеню окиснення Маґнію. –
Вправа 3
Хімічний зв'язок – це зв’язок між частинками речовини, який утримує їх разом у молекулі або кристалі.
Електрони незавершеного енергетичного рівня називають валентними.
Атоми (за винятком елементів першого періоду) прагнуть досягти енергетично вигідного стану, доповнивши зовнішній енергетичний рівень електронами до восьми, що є характерним для атомів інертних елементів.
Довжина зв'язку – це відстань між ядрами двох атомів, що утворюють хімічний зв’язок.
Чим менша довжина зв'язку, тим міцніший зв'язок між атомами.
Енергія зв'язку – це кількість енергії, необхідна для розриву хімічного зв’язку між двома атомами.
Вона є показником міцності зв’язку та його стійкості до розриву.
Заповніть схему.
| ВИДИ ХІМІЧНОГО ЗВ'ЯЗКУ |
| Ковалентний |
Йонний |
| О2 |
NaCl |
|
Зв’язок між атомами з
утворенням спільних
електронних пар
|
Зв’язок між йонами утворений
унаслідок електростатичної
взаємодії між ними
|
Сторінка 66
Вправа 4
1. Запишіть електронні формули та сформулюйте гіпотезу про можливість утворення йонів для пар атомів:
Калію та Хлору, Кальцію та Оксигену, Барію та Магнію, Бору та Нітрогену, Сульфуру та Гідрогену.
K+Cl–, Ca2+O2–
Гіпотеза. Йони утворюються між атомами металічних і неметалічних елементів, бо їхні атоми здатні віддавати і приєднувати електрони, набуваючи електронної оболонки атомів інертних елементів, утворюючи таким чином стійкий хімічний зв'язок.
| Пари атомів |
Можливість утворення йонів
(так/ні)
|
Передача електронів
(де можливо)
|
| K, Cl |
так |
віддає 1 електрон,
приєднує 1 електрон
|
| Ca, O |
так |
віддає 2 електрони,
приєднує 2 електрони
|
| Ba, Mg |
ні |
– |
| B, N |
ні |
– |
| S, H |
ні |
– |
Наша гіпотеза
підтвердилася.
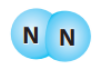
2. Запишіть довжину зв'язку для моделей молекул.
| Сполуки |
Водень |
Кисень |
Азот |
Хлор |
|
Моделі
молекул
|
 |
 |
 |
 |
|
Енергія
зв'язку
|
432
кДж/моль
|
493
кДж/моль
|
941
кДж/моль
|
243
кДж/моль
|
3. Енергія зв'язу в молекулі водню становить 432 кДж/моль, а в молекулі хлору – 243 кДж/моль. Яка молекула є стійкішою?
Стійкішою є молекула водню, бо має вище значення енергії зв'язку у порівнянні зі значенням в молекулі хлору.
Вправа 5
Підбиваємо підсумки. Чим менша довжина зв’язку, тим вище значення енергії зв'язку.
Сторінка 67
§31 Модель ковалентного хімічного зв'язку.
Полярний і неполярний ковалентний зв'язки
Вправа 2
1. Хімічний зв’язок може утворюватися лише унаслідок переміщення електронів від одного атома до іншого. –
2. Йони утворюються внаслідок переміщення електронів від одного атома до іншого. +
3. Усі хімічні зв’язки мають однаковий механізм утворення. –
4. Ковалентний зв’язок утворюється за рахунок утворення спільної електронної пари. +
5. Чим коротший хімічний зв’язок, тим він слабший. –
6. Довжина хімічного зв’язку впливає на його міцність. +
7. Йонний зв’язок утворюється між атомами неметалічних елементів. –
8. Енергія зв’язку характеризує міцність хімічного зв’язку між атомами. +
9. Молекула кисню утворена ковалентним зв’язком між атомами Оксиґену. +
Вправа 3
Полярний ковалентний зв'язок виникає між атомами неметалічних елементів з різною електронегативністю елементів.
Чим більшу електронегативність матиме атом, тим сильніше притягує до себе валентні електрони.
Якщо один атом притягує електрони сильніше, ніж інший, це призводить до утворення часткових зарядів на атомах: один атом набуває негативного заряду (аніон), а інший – частково позитивного заряду (катіон).
Спільна електронна пара в молекулі HCl зміщена в бік атома Хлору.
Полярність молекул впливає на їх фізичні властивості:
• добра розчинність;
• вища температура плавлення;
• вища температура кипіння.
| ВИДИ КОВАЛЕНТНОГО ЗВ'ЯЗКУ |
| Неполярний |
Полярний |
|
атоми однакових
неметалічних елементів
(I2, Cl2, O2, N2)
|
атоми різних
неметалічних елементів
(HCl, CO, CO2 , N2O)
|
|
спільні електронні пари
рівновіддалені від ядер
обох атомів
|
спільні електронні пари
зміщені в бік більш
електронегативного атома
|
Сторінка 68
|
Гіпотеза
|
План експерименту
|
Очікуванні результати
|
|
Кисень можна добути
шляхом розкладу
гідроген пероксиду
під дією манган
(IV) оксиду, який є
каталізатором.
|
1. У колбу налити 3-5 мл
розчину гідроген пероксиду.
2. Додати невелику кількість
каталізатора манган (IV) оксиду.
3. Зібрати кисень.
|
Отримаємо кисень і
воду.
|
Сторінка 69
§32 Кристалічні й аморфні речовини
Вправа 2
1. Хімічні зв’язки визначають фізичні та хімічні властивості речовин. +
2. У молекулі HCl атоми зв’язані полярним ковалентним зв’язком. +
3. Гідроґен хлорид добре розчинний у воді. +
4. У молекулі води атоми Гідроґену і Оксиґену зв’язані неполярним ковалентним зв’язком. -
5. Неполярний ковалентний зв’язок утворюється між однаковими атомами неметалічних елементів. +
6. У молекулі Cl2 атоми зв’язані полярним ковалентним зв’язком і утворюють дві спільні електронні пари. -
7. Амоніак (NH3) погано розчиняється у воді. -
8. Під час утворення полярного ковалентного зв’язку спільна електронна пара зміщується до більш електронегативного атома. +
9. У молекуля гідроген сульфіду спільні електронні пари зміщені до атома Сульфуру. +
Вправа 3
| Будова твердих речовин |
| Кристалічна |
Аморфна |
|
структурні частинки речовини
розміщуються впорядковано
|
структурні частинки речовини
розміщуються невпорядковано
|
|
Властивості
|
|
Однорідність властивостей,
дуже висока температура
плавлення
|
Властивості можуть варіюватися,
широкий діапазон температур
плавлення
|
|
Приклади
|
|
Сіль, цукор, кварц, алмаз, пісок
|
Ґума, смола, віск, скло, пластмаса
|
2 Речовини: кристалічні (сіль, цукор, мідний дріт, пісок) і аморфні (скла, пластмаса, віск, ґума).
4 Порівняйте властивості досліджених речовин.
|
Властивість
|
Кристалічні
речовини
|
Аморфні
речовини
|
Висновки щодо струк-
тури та властивостей
|
|
Аналіз
структури
|
Регулярна,
повторювана
ґратка
|
Безладно, не
впорядкована
|
Кристалічні речови мають
характерну регулярну
повторювану ґратку і
однорідність
властивостей.
Аморфні речовини мають
невпорядковану структуру,
властивості можуть
варіюватися.
|
| Твердість |
різна |
різна |
| Електропровідність |
проводять і
не проводять
|
не проводять |
| Теплопровідність |
вища |
нижча |
|
Оптичні
властивості
|
різні |
різні |
| Розчинність у воді |
різна |
різна |
§33 Модель йонного зв'язку. Йонні кристали
Вправа 2
1. Усі кристалічні речовини мають однакову геометричну форму. -
2. У аморфних речовин частинки розташовані у правильному порядку. -
3. Сіль і цукор — приклади аморфних речовин. -
4. Скло є аморфною речовиною. +
5. Під час плавлення аморфних речовин важко зафіксувати температуру плавлення. +
6. Усі тверді речовини є кристалічними. -
7. Парафін і пластмаса — це кристалічні речовини. -
8. У кристалічних речовинах частинки упорядковані регулярну, повторювану тривимірну структуру, що утворює кристалічну ґратку. +
9. Аморфні речовини зазвичай прозорі й блискучі. -
Вправа 3
Йонний зв’язок — це вид хімічного зв’язку, що виникає внаслідок електростатичної взаємодії між йонами з протилежними зарядами: катіонами й аніонами. Утворюється в результаті повної передачі одного або кількох електронів від атома металічного елемента до атома неметалічного елемента. Як наслідок, утворюються йони з різними зарядами, які взаємно притягуються, що й забезпечує стійкість йонної сполуки.
Йонні сполуки мають високу температуру плавлення і кипіння. Не проводять електричний струм у твердому стані, але проводять у розчинах чи розплаві. Більшість розчинні у воді. Йонні кристали крихкі та можуть легко розламатися під механічним навантаженням. Тверді завдяки міцним йонним зв'язкам.
Заповність схему
| Ковалентний неполярний |
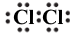 |
| ковалентний полярний |
|
надлишковий, або
ефективний
позитивний заряд
|
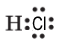 |
надлишковий, або
ефективний
негативний заряд
|
| Йонний |
| Na+Cl- |
§34 Фізичні властивості атомних і молекулярних кристалів
Вправа 2
1. Йонний зв’язок виникає між атомами металічного і неметалічного елемента. +
2. У йонному зв’язку атоми спільно використовують електрони. -
3. Аніони — це частинки з негативним зарядом. +
4. Йонні сполуки не проводять електричний струм у розплавах і розчинах. -
5. Йонний зв’язок — це результат електростатичного притягання протилежно заряджених йонів. +
6. Йонні кристали легко плавляться. -
7. Під час утворення катіону атом втрачає електрон. +
8. Йонні сполуки добре розчиняються у воді. +
9. Йонний зв’язок є слабшим за ковалентний. -
Вправа 3
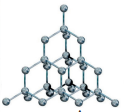
Атомні кристали утворені ковалентними зв’язками, які виникають між атомами в усіх напрямках, що створює суцільну тривимірну сітку.
Це призводить до утворення дуже міцних і стійких структур.
Приклад: алмаз, графіт, силіцій
| |
Алмаз |
Графіт |
| Структура |
Атомні кристали
|
Атомні кристали
|
|
|
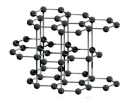
|
| Властивості |
Дуже твердий, нерозчинний
у воді, не проводить
електричний струм
|
М'який завдяки шаруватій
структурі, нерозчинний у воді,
проводить електричний струм
|
Сторінка 74
Вправа 4
ДОСЛІДЖУЄМО речовини.
4 Заповнюємо таблицю.
|
Фізичні
властивості
|
Речовина |
| Цукор |
Кухонна сіль |
Графіт |
| Колір |
безбарвний
(в масі білий)
|
безбарвний
(в масі біла)
|
чорний
|
| Блиск |
відсутній |
відсутній |
наявний |
| Запах |
відсутній |
відсутній |
відсутній |
|
Розчинність у воді
|
розчинний |
розчинна |
нерозчиний |
| Міцність |
крихкий |
крихка |
міцний |
|
Температура плавлення
|
низька |
висока |
дуже висока |
|
Типи кристалічної ґратки
|
молекулярна |
йонна |
атомна |
5. Нашу гіпотезу підтверджено. Кухонна сіль має йонну будову, цукор має молекулярну будову, а графіт має атомну будову.





