Інші завдання дивись тут...
© 8next.com (відповіді, перероблене і доповнене)
Думаймо
Чим орбіталь відрізняється від орбіти?
Орбіталь відрізняється від орбіти тим, що є частиною простору (тривимірний), де найімовірніше (вище 90%) перебуває електрон, тоді як орбіта — це траєкторія руху небесного тіла на площині (двовимірна).
Іншими словами, орбіталь описує квантовий стан електрона і не має фізичної траєкторії, на відміну від класичного поняття орбіти.
Думаймо
Атом якого хімічного елемента має електронну формулу, наведену на малюнку 77?
Електронну формулу 1s1 має атом Гідрогену (Н).
Думаймо
1. Яка максимальна кількість електронів може перебувати на 3s–підрівні, 3p–підрівні, 3d–підрівні?
Максимальна кількість електронів на 3s–підрівні — 2, на 3p–підрівні — 6, на 3d–підрівні — 10.
2. Скільки d–орбіталей належить третьому енергетичному рівню?
Оскільки на 3d–підрівні максимально міститься 10 електронів, а на одній орбіталі — 2 електрони, то на третьому енергетичному рівні міститься 5 d–орбіталей (10:2=5).
Виконаймо вправу
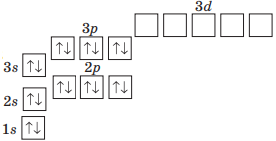
Запишіть електронну формулу третього енергетичного рівня, цілком заповненого електронами, а також зобразіть її графічний варіант.
Електронна формула заповненого третього рівня: 1s22s22p63s23p6.
Графічний варіант:
ВИОКРЕМЛЮЄМО ОСНОВНЕ
Проаналізувавши матеріал, викладений у параграфі, запишіть у зошиті висновки про електрон, енергію електронів та їх розміщення в атомах.
Електрон одночасно виявляє властивості і частинки, і хвилі. Подібно до інших частинок, електрон має певну масу й заряд. Разом з тим під час руху електрон виявляє хвильові властивості, тому характеризується енергією. Орбіталі заповнюються електронами за принципом «мінімальної енергії»: спочатку заповнюється перший енергетичний рівень, потім — другий та третій. Якщо на одному енергетичному підрівні містяться декілька електронів, то вони розподіляються таким чином, щоб число неспарених електронів було максимальним.
Думаймо
Сформулюйте цікаве запитання за темою параграфа і поставте його своїм однокласникам / однокласницям.
Чому в атомі Літію електрон, що міститься на другому енергетичному рівні, перебуває на s–орбіталі, а не на р–орбіталі?
Сферична s–орбіталь компактніша та енергетично вигідніша за гантелеподібну p–орбіталь.
ВАШІ ДОСЯГНЕННЯ ТА ВІДКРИТТЯ
Вправа 298
Чим електрон відрізняється від фізичного тіла?
Електрон відрізняється від фізичного тіла тим, що під час руху виявляє хвильові властивості. Через це для електрона неможливо водночас визначити швидкість руху та напрямок, тому неможливо визначити, якою траєкторією рухається електрон в атомі.
Вправа 299
Яку частину атома називають орбіталлю? Охарактеризуйте форми s– і p–орбіталей та їх розміщення в атомі.
Частину простору в атомі, де перебування електрона є найбільш імовірним, називають орбіталлю.
Форма s–орбіталі — сферична. У центрі такої орбіталі розміщене ядро атома.
Форма р–орбіталі — гантелеподібна. Такі орбіталі зорієнтовані в атомі перпендикулярно одна до одної вздовж осей координат х (позначення — px–орбіталь), у (py–орбіталь) і z (pz–орбіталь), в точці перетину координат (місце звуження гантелей) розміщене ядро атома.
Узгодьте кожне позначення з його змістом:
|
1. 
2. 
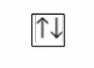
3. 
|
а) заповнена орбіталь;
б) спарені електрони;
в) неспарений електрон;
г) порожня (вакантна) орбіталь;
д) електрони з протилежними спінами.
|
Відповідь: 1 — г), 2 — в), 3 — а), б), д).
Вправа 301
Енергія якого електрона менша — розміщеного в p–орбіталі 2–го енергетичного рівня чи в s–орбіталі 3–го енергетичного рівня?
Менша енергія електрона, розміщеного в р–орбіталі 2–го енергетичного рівня на відміну від s–орбіталі 3–го енергетичного рівня, бо 2–ий енергетичний рівень розміщений ближче до ядра, ніж 3–ій.
Вправа 302
Назвіть характеристики, за якими один електрон може відрізнятися від іншого.
Один електрон відрізняються енергією, формою орбіталі (s,p,d,f), її просторовою орієнтацією та напрямком спіну.
Вправа 303
Чому в позначенні s–орбіталі немає індексу (наприклад, sx)?
У позначенні s–орбіталі немає індексу, бо s–орбіталь є сферичною і в просторі має вигляд кулі з ядром атома в центрі координат, а не розміщується на одній з осей координат як, наприклад р–орбіталь. Дивись вправу 299.
Вправа 304
Проаналізуйте твердження. Чи є з–поміж них правильні?
І. Електрони атома, які перебувають в орбіталях однакової форми та об’єму, мають однакову енергію.
ІІ. Максимальна кількість електронів на кожному енергетичному рівні та підрівні є парною.
Відповідь: В. Обидва правильні.
Пояснення. Твердження I правильне, бо мова йде про електрони в орбіталях однакової форми одного рівня (а не різних), наприклад, 2pх,2pу,2pz. Твердження II правильне, бо максимальна кількість електронів на енергетичному рівні визначається за формулою 2n², а на підрівні — добутком кількості орбіталей і числа 2, тому завжди є парною.
Вправа 305
Який запис, на вашу думку, надає більше інформації про електрони, що містяться в атомі — електронна формула чи її графічний варіант? графічний варіант формули.
Чому?
Електронна формула надає інформацію про кількісний розподіл електронів по орбіталях енергетичних рівнів і підрівнів (номери енергетичних рівнів, типи електронних орбіталей та кількість електронів в орбіталі), а її графічний варіант ще додатково надає інфармацію про просторове розміщення електронів на орбіталях всередині кожного підрівня (спарені чи неспарені електрони), їхню орієнтацію (спін) та наявність вільних орбіталей.
Вправа 306
Серед указаних підрівнів назвіть ті, які в атомі неможливі: 6p, 2d, 1p, 5s.
Неможливий підрівень 2d, бо 2–ий енергетичний рівень не містить d–підрівнів, а має тільки s– i p–підрівні.
Неможливий підрівень 1р, бо 1–ий енергетичний рівень не має p–підрівнів, а має тільки s–підрівень.
Вправа 307
Випишіть ключові слова і словосполучення з тексту параграфа для укладання двомовного словничка.
Орбіталь — orbital, s–орбіталь — s–orbital, р–орбіталь — p–orbital, електронна оболонка — electron shell, енергетичний рівень — energy level, енергетичний підрівень — energy sublevel, спін електрона — electron spin.
Вправа 308
Створіть у зошиті таблицю оцінювання ваших знань і заповніть її.
| Навчальні досягнення (що я знаю та вмію) |
Самооцінка |
| Знаю особливу природу електрона. |
... |
| Знаю, що називають атомною орбіталлю. |
... |
| Можу описати форму та просторову орієнтацію s– та р–орбіталей. |
... |
| Вмію визначати максимальну кількість електронів на енергетичному рівні (2n²). |
... |
| Вмію складати електронні та графічні формули атомів перших 20–ти елементів періодичної таблиці. |
... |
––––––––– ПРОГРАМА 2016 року і 2021 року ––––––––––
§6 2016 / §5 2021 СУЧАСНА МОДЕЛЬ АТОМА
Вправа 38 / 29 (2021)
Що таке орбіталь? Частину простору в атомі, де перебування електрона наймовірніше, називають орбіталлю.
Які форми мають s– і р– орбіталі? S–орбіталь має форму кулі (сферичну), р–орбіталь має форму об'ємної вісімки (гантелі, причому ядро атома міститься у місці звуження гантелі).
Порівняйте за змістом термін "орбіталь" і слово "орбіта". Термін "орбіталь" означає частину простору в атомі, а слово "орбіта" ― траєкторію руху тіла навколо чогось.
Вправа 39 / 30 (2021)
Як розміщені у просторі р–орбіталі одного атома? У просторі вздовж осей х, у, z, тому їх ще називають Рх–, Ру–, Рz–орбіталями.

Чому в позначенні s–орбіталі немає індексу (наприклад, Sх)? Бо s–орбіталь не розміщується в просторі на одній з осей координат (наприклад, х), а є сферичною, в центрі координат розміщене ядро атома.

Вправа 40 / 31 (2021) Знайдіть відповідність.
|
1. 
2. 

3.
|
а) заповнена орбіталь;
б) спарені електрони;
в) електрони з протилежними
спінами;
г) неспарений електрон;
д) порожня вакантна орбіталь.
|
Відповідь: 1–д), 2–г), 3–а),б),в)
Вправа 41 / 32 (2021)
Назвіть характеристики, за якими один електрон може відрізнятися від іншого чи бути подібним до нього. Формою орбіталі, спіном, енергією.
Вправа 42 / 33 (2021)
Енергія якої частинки менша: s–електрона на 1–му енергетичному рівні чи р–електрона на 2–му енергетичному рівні? s–електрона на 1–му енергетичному рівні.
Відповідь поясніть. Чим компактніша орбіталь і чим ближче до ядра перебуває електрон, тим його енергія менша, тому енергія s–електрона на 1–му енергетичному рівні менша від енергії р–електрона на 2–му енергетичному рівні.
Вправа 43 / 34 (2021)
Чи завжди енергія електрона 3–го енергетичного рівня більша, ніж електрона 2–го рівня? Завжди, бо електрони першого енергетичного рівня мають найменшу енергію, другого ― вищу, а третього ― ще вищу.
Чи зміниться відповідь, якщо порівнювати енергію електрона 4–го рівня і електрона 3–го рівня? Використайте схему 2. Зміниться. Енергія s–електрона 4–го рівня (4s–підрівня) менша від енергії d–електрона 3–го рівня (3d–підрівня), хоча в даному випадку d–підрівень розташований на ближчому до ядра енергетичному рівні.
Вправа 44 / 35 (2021)
Який запис дає більше інформації про електрони: електронна формула чи її графічний варіант? Графічний варіант.
Чому? Дає інформацію не лише про розподіл електронів по орбіталях, а й показує неспарені (валентні) електрони, наявність вакантних орбіталей.
Вправа 45 / 36 (2021)
Серед указаних підрівнів назвіть ті, які в атомі неможливі: 6р, 2d, 1р, 5s.
2d, бо другий енергетичний рівень (вказує коефіцієнт перед буквою) не має d–підрівня, а має тільки s– i p–підрівні.
1р, бо перший енергетичний рівень не має p–підрівня, а має тільки s–підрівень.
Інші завдання дивись тут...