Інші завдання дивись тут...
© 8next.com (відповіді, перероблене і доповнене)
Експериментуймо
Узявши до уваги, що кожний електрон намагається зайняти вільну орбіталь підрівня, а в разі її відсутності «підселяється» в орбіталь до іншого електрона, складіть електронні формули атомів Нітрогену, Оксигену, Флуору та Неону, а також зобразіть графічні варіанти цих формул.
|
Елемент
|
Електронна формула
|
Графічний варіант
|
| Нітроген |
7N 1s22s22p3, або [He]2s22p3 |
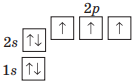 |
| Оксиген |
8O 1s22s22p4, або [He]2s22p4 |
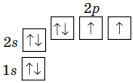 |
| Флуор |
9F 1s22s22p5, або [He]2s22p5 |
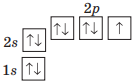 |
| Неон |
10N 1s22s22p6, або [He]2s22p6 |
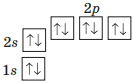 |
Думаймо
Запропонуйте гіпотезу, чому розміри атомів хімічних елементів у періоді зменшуються, а не збільшуються.
Атоми елементів одного періоду мають однакову кількість енергетичних рівнів з електронам, але заряди ядер атомів у періоді збільшуються. Що більший заряд ядра, тим ближче до нього перебувають електрони і зменшується радіус атома.
Експериментуймо
Складіть електронні формули атомів решти хімічних елементів 3–го періоду від Магнію до Аргону.
Магній 12Mg 1s22s22p63s2, або [Ne]3s2
Алюміній 13Al 1s22s22p63s23p1, або [Ne]3s23p1
Силіцій 14Si 1s22s22p63s23p2, або [Ne]3s23p2
Фосфор 15P 1s22s22p63s23p3, або [Ne]3s23p3
Сульфур 16Si 1s22s22p63s23p4, або [Ne]3s23p4
Хлор 17Cl 1s22s22p63s23p5, або [Ne]3s23p5
Аргон 18Ar 1s22s22p63s23p6, або [Ne]3s23p6
Експериментуймо
Запишіть електронну формулу атома елемента № 20 Кальцію.
20Са 1s22s22p63s23p64s2, або [Ar]4s2
Думаймо
До s– чи р–елементів належать Сульфур, Барій, Калій, Неон, Йод?
До s–елементів належать елементи головних підгруп I та II груп періодичної таблиці, тому Калій (К) і Барій (Ва).
До р–елементів належать елементи головних підгруп III—VIII груп періодичної таблиці, тому Сульфур (S), Неон (Ne), Йод (I).
У короткій формі періодичної таблиці (див. форзац 1) клітинки з s–елементами зазвичай фарбують у рожевий колір, а з р–елементами — у блакитний.
Думаймо
Назвіть неметалічні елементи 1—2–го періодів, які є винятками.
Винятками є атоми елементів 1–го періоду: Гідроген Н, що має 1 зовнішній електрон, Гелій Не, що має 2 зовнішні електрони, і атом елемента 2–го періоду: Бор В, що має 3 зовнішні електрони, бо атоми неметалічних елементів зазвичай мають від 4–х до 8–ми зовнішніх електронів.
Проаналізувавши матеріал, викладений у параграфі, запишіть у зошиті висновки про особливості електронної будови атомів хімічних елементів № 1—20 і послідовність заповнення електронами орбіталей у цих атомах.
Кількість енергетичних рівнів атома хімічного елемента збігається з номером періоду періодичної таблиці.
Кількість зовнішніх електронів в атомі хімічного елемента дорівнює номеру головної підгрупи групи в короткому варіанті періодичної таблиці.
Електрони заповнюють енергетичні рівні та підрівні за принципом мінімальної енергії (від найменшої до найбільшої): 1s→2s→2p→3s→3p→4s→3d→4р, що забезпечує максимальну стійкість атома.
Думаймо
Сформулюйте цікаве запитання за темою параграфа і поставте його своїм однокласникам/однокласницям.
Чому в атомах елементів четвертого періоду починає заповнюватися електронами четвертий енергетичний рівень, незважаючи на те що третій рівень ще неповний?
Це пов’язано з тим, що енергія 4s–підрівня менша, ніж енергія 3d–підрівня, хоча в цьому випадку d–підрівень розташований на ближчому до ядра електронному рівні.
ВАШІ ДОСЯГНЕННЯ І ВІДКРИТТЯ
Вправа 309
Назвіть елемент, атом якого має таку електронну формулу:
а) 1s22s22p63s23p2;
Сума електронів у записі електронної формули атома елемента чисельно дорівнює його порядковому номеру, тому знаходимо суму електронів і визначаємо відповідний елемент. Всього 14 (2+2+6+2+2=14) електронів, тому порядковий номер 14. Цим хімічним елементом є Силіцій (Si);
б) [Нe]2s22p5;
Електронна формула зовнішнього енергетичного рівня ...2s22p5. Заповнюється другий енергетичний рівень, значить, елемент розташований у 2–му періоді. На зовнішньому енергетичному рівні атома 7 (2+5=7) електронів, отже, елемент розташований у VІІ групі, це р–елемент, тому — в головній підгрупі. Шукаємо в періодичній таблиці клітинку на перетині 2–го періоду й VII групи. Цим хімічним елементом є Флуор (F);
в) [Ar]4s2.
Електронна формула зовнішнього енергетичного рівня ...4s2. Заповнюється четвертий енергетичний рівень, значить, елемент розташований у 4–му періоді. На зовнішньому енергетичному рівні атома 2 електрони, отже, елемент розташований у ІI групі, це s–елемент, тому — в головній підгрупі. Шукаємо в періодичній таблиці клітинку на перетині 4–го періоду й II групи. Цим хімічним елементом є Кальцій (Са).
Вправа 310
Атом на другому енергетичному рівні має 6 електронів. Скільки серед них спарених, а скільки — неспарених?
Із шести електронів на останньому (другому) енергетичному рівні ...2s22p4 є 2 s–електрони, які є спареними, тому 4 (6–2=4) електрони є р–електронами, з них, два р–електрони спарені і два р–електрони неспарені. Отже, разом є чотири спарених електронів (дві пари) і два неспарених електрони.
Вправа 311
Атоми яких елементів 2–го періоду мають один неспарений електрон, два неспарені електрони?
На кількість зовнішніх електронів в атомі елемента вказує номер групи періодичної таблиці. Беручи до уваги, що заповнена орбіталь містить 2 електрони, робимо висновок, що елементи непарних груп (крім V) будуть мати один неспарений електрон.
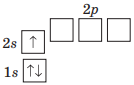
Один неспарений електрон мають атоми таких хімічних елементів 2–го періоду:
| Літій (I група) |
Бор (III група) |
Флуор (VII група) |
 |
 |
 |
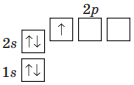
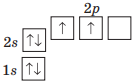
Два неспарені електрони мають атоми таких хімічних елементів 2–го періоду (крім Неону):
| Карбон (IV група) |
Оксиген (VI група) |
 |
 |
Вправа 312
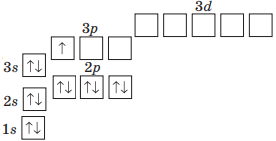
Укажіть хімічний елемент, електронну будову атома якого описує така графічна формула:
Графічна формула містить три енергетичні рівні, значить, елемент розташований у 3–му періоді. На останньому енергетичному рівні є 2 s–електрони та 1 р–електрон, разом 3 зовнішні електрони, отже, елемент розташований у ІІІ групі, це р–елемент, тому — в головній підгрупі. Шукаємо в періодичній таблиці клітинку на перетині 3–го періоду й ІІІ групи. Цей елемент — Алюміній Al.
Або міркуємо ще так:
сума електронів у записі графічної формули атома елемента чисельно дорівнює його порядковому номеру, тому знаходимо суму електронів і визначаємо відповідний елемент. Всього 13 (2+2+6+2+1=13) електронів, тому порядковий номер 13. Цим хімічним елементом є Алюміній Al.
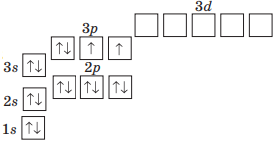
Графічна формула містить три енергетичні рівні, значить, елемент розташований у 3–му періоді. На останньому енергетичному рівні є 2 s–електрони та 4 р–електрони, разом 6 зовнішніх електронів, отже, елемент розташований у VІ групі, це р–елемент, тому — в головній підгрупі. Шукаємо в періодичній таблиці клітинку на перетині 3–го періоду й VІ групи. Цей елемент — Сульфур S.
Або міркуємо ще так:
сума електронів у записі графічної формули атома елемента чисельно дорівнює його порядковому номеру, тому знаходимо суму електронів і визначаємо відповідний елемент. Всього 16 (2+2+6+2+4=16) електронів, тому порядковий номер 16. Цим хімічним елементом є Сульфур S.
Вправа 313
Укажіть помилки в електронних формулах атомів:
а) 1s22s32p1;
Максимальна кількість s–електронів може бути 2, тому помилка в кількості s–електронів на 2–му енергетичному рівні атома елемента. Отже, правильна формула має вигляд: 1s22s22p1.
б) [Ar]3s23p2;
Останнім є третій енергетичний рівень, тому в дужках має бути символ хімічного елемента 2–го періоду головної підгрупи VIII групи — Неону. Отже, правильна формула має вигляд [Ne]3s23p2.
в) 1s22s22p63s13p4.
Максимальна кількість s–електронів може бути 2, тому помилка в кількості s–електронів на 3–му енергетичному рівні. Отже, правильна формула має вигляд 1s22s22p63s23p4.
Вправа 314
Скориставшись періодичною таблицею, з’ясуйте:
а) яких елементів більше — p–елементів чи d–елементів;
У періодичній таблиці р–елементи перебувають у головних підгрупах III–VIII груп, а d–елементи — у побічних підгрупах I–VIII груп. Тому очевидним є те, що d–елементів (40) є більше, ніж р–елементів (36).
б) які елементи — металічні чи неметалічні — переважають серед s–елементів, p–елементів.
Серед s–елементів переважають металічні елементи, бо це хімічні елементи I i II групи, а також побічних підгруп I–VIII груп.
Серед р–елементів переважають неметалічні елементи, бо це хімічні елементи головної підгрупи III–VIII груп.
Вправа 315*
Назвіть два елементи, в атомах яких кількість електронів у всіх s–орбіталях така сама, що й у р–орбіталях.
Оксиген (О). Електронна формула 1s22s22p4, отже, має 4 електрони на двох s–орбіталях і 4 електрони на р–орбіталі.
Магній (Mg). Електронна формула 1s22s22p63s2, отже, має 6 електронів на трьох s–орбіталях і 6 електронів на р–орбіталі.
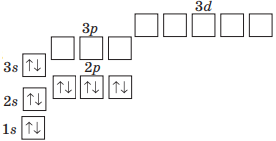
| Оксиген (O) |
Магній (Mg) |
 |
 |
Вправа 316
Випишіть ключові слова і словосполучення з тексту параграфа для укладання двомовного словничка.
Зовнішні електрони — outer electrons, s–елементи — s–elements, p–елементи — р–elements, d–елементи — d–elements, f–елементи — f–elements.
Вправа 471
Створіть у зошиті таблицю оцінювання ваших знань і заповніть її.
| Навчальні досягнення (що я знаю та вмію) |
Самооцінка |
| Знаю принцип «мінімальної енергії», що визначає будову атома. |
... |
| Вмію складати повні та скорочені електронні формули атомів. |
... |
| Вмію класифікувати елементи за типами орбіталей (s–, р–, d–, f–елементи). |
... |
| Вмію визначити характер елемента за кількістю зовнішніх електронів. |
... |
––––––––– ПРОГРАМА 2016 року і 2021 року ––––––––––
§7 / §6. ЕЛЕКТРОННА БУДОВА АТОМІВ
Вправа 46 / 37 (2021)
Атом елемента 2–го періоду на останньому енергетичному рівні має 6 електронів. Скільки серед них спарених електронів, а скільки — неспарених? 4 спарених і 2 неспарених.
Цим атомом є Оксиген, электронна формула якого 1s22s22p4, а графічна має вигляд:

Вправа 47 / 38 (2021)
Атоми яких елементів 2–го періоду мають:
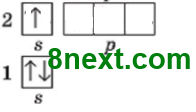
а) один неспарений електрон; Літій, Бор, Флуор
|
Літій 1s22s1
|
Бор 1s22s22p1

|
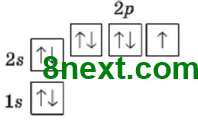
Флуор F 1s22s22p5
|
б) два неспарені електрони? Карбон, Оксиген
|
Карбон 1s22s12p2
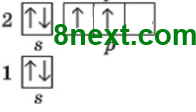
|
Оксиген 1s22s22p4

|
Вправа 39 (2021)
Назвіть елемент, атом якого має таку електронну формулу:
а) 1s2; Гелій
Сума електронів у записі електронної формули атома елемента чисельно дорівнює його порядковому номеру, тому знаходимо суму електронів і визначаємо відповідний елемент. Всього 2 електрони, тому №2 — це Гелій;
б) 1s22s22p63s1; Натрій
Сума електронів у записі електронної формули атома елемента чисельно дорівнює його порядковому номеру, тому знаходимо суму електронів і визначаємо відповідний елемент. Всього 11 (2+2+6+1=11) електронів, порядковий №11 — це Натрій;
в) [Ne]3s2. Магній
Електронна формула зовнішнього енергетичного рівня ...3s2. Заповнюється третій рівень, значить, елемент розташований у 3–му періоді. В атомі елемента на зовнішньому енергетичному рівні 2 електрони, отже, елемент розташований у ІI групі, це s–елемент, тому — в головній підгрупі. Шукаємо в Періодичній таблиці клітинку на перетині 3–го періоду й II групи. Цей елемент — Магній.
Вправа 48
Назвіть елемент, атом якого має таку електронну формулу:
[Ne]3s1. Натрій
Електронна формула зовнішнього енергетичного рівня ...3s1. Заповнюється третій рівень, значить, елемент розташований у 3–му періоді. В електронній оболонці атома елемента на зовнішньому рівні 1 електрон, отже, елемент розташований у І групі, це s–елемент, тому — в головній підгрупі. Шукаємо в Періодичній таблиці клітинку на перетині 3–го періоду й I групи. Цей елемент — Натрій.
Вправа 49 / 40 (2021)
Назвіть два елементи, в атомах яких кількість усіх s– і всіх р–електронів однакова.
Оксиген. Електронна формула 1s22s22p4 містить 4 s–електрони і 4 р–електрони
Магній. Електронна формула 1s22s22p63s2 містить 6 s–електронів і 6 р–електронів
Вправа 41 (2021)
Укажіть хімічний елемент, електронну будову атома якого описує графічна формула в підручнику.
а) Aлюміній Аl
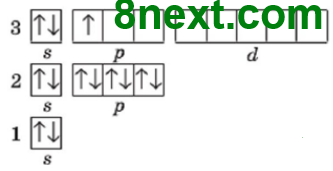
Графічна формула містить три енергетичні рівні, значить елемент розташований у 3–му періоді. На останньому (3) енергетичному рівні є 2 s–електрони та 1 р–електрон, разом три зовнішні електрони, отже, елемент розташований у ІІІ групі, це р–елемент, тому — в головній підгрупі. Шукаємо в Періодичній таблиці клітинку на перетині 3–го періоду й ІІІ групи. Цей елемент — Алюміній Al.
б) Сульфур S
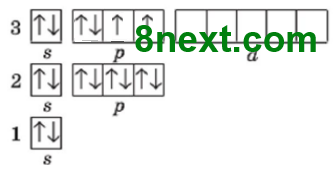
Графічна формула містить три енергетичні рівні, значить елемент розташований у 3–му періоді. На останньому (3) енергетичному рівні є 2 s–електрони та 4 р–електрони, разом шість зовнішніх електронів, отже, елемент розташований у VІ групі, це р–елемент, тому — в головній підгрупі. Шукаємо в Періодичній таблиці клітинку на перетині 3–го періоду й VІ групи. Цей елемент — Сульфур S.
Вправа 50
Яке значення валентності може мати елемент, якщо його атом має електронну формулу:
а) 1s22s22p63s23p3; Три
В електронній формулі на останньому (3) енергетичному рівні є 2 s–електрони, які є спареними, та 3 р–електрони, які є неспареними. На можливе значення валентності елемента вказує кількість неспарених електронів в електронній оболонці атома, тому може бути валентність три;
б) [Ne]3s23p5? Один
В електронній формулі на останньому (3) енергетичному рівні є 2 s–електрони, які є спареними, та 5 р–електронів, з яких 4 р–електрони є спареними і 1 р–електрон — неспареним. На можливе значення валентності елемента вказує кількість неспарених електронів в електронній оболонці атома, тому може бути валентність один.
Інші завдання дивись тут...