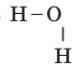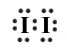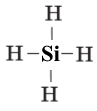Експериментуймо
Електронна формула атома Гідрогену: 1Н 1s1
Графічний варіант:
![]()
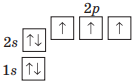
Електронна формула атома Нітрогену: 7N 1s22s22p3, або [He]2s22p3
Графічний варіант:
Проаналізувавши матеріал, викладений у параграфі, запишіть у зошиті висновки про те, електронні оболонки якого складу забезпечують стійкість атомів і як сполучені атоми в молекулах неметалів.
Стійкість атомів забезпечують електронні оболонки, що мають вісім електронів, так званий, електронний октет ns2np6 (для першого періоду — 1s2). У молекулах неметалів атоми сполучені ковалентними зв’язками шляхом утворення спільних електронних пар за рахунок неспарених електронів цих атомів.
Вправа 327
Графічний варіант атома Хлору:
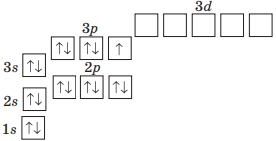
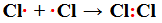
|
Повна електронна формула |
Спрощена електронна формула |
Графічна формула |
|
|
|
|
Вправа 329
На малюнку 82 зображено модель молекули білого фосфору P4. З якою кількістю атомів сполучений кожний атом у цій молекулі? Простими, подвійними чи потрійними є ковалентні зв’язки між атомами в молекулі P4?
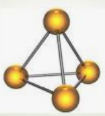
|
Повна електронна формула |
Спрощена електронна формула |
Графічна формула |
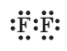 |
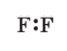 |
|
Вправа 331
 |
| Навчальні досягнення (що я знаю та вмію) | Самооцінка |
| Знаю електронну будову атомів інертних елементів. | ... |
| Знаю механізм утворення ковалентного зв'язку у простих речовинах. | ... |
| Вмію розрізняти ковалентний зв'язок за кратністю (простий, подвійний, потрійний) | ... |
| Вмію складати електронні і структурні формули простих речовин. | ... |
––––––––– ПРОГРАМА 2016 року і 2021 року––––––––––
§15 КОВАЛЕНТНИЙ ЗВ'ЯЗОК
Вправа 98 / 88 (2021)
Який зв'язок називають ковалентним? Хімічний зв'язок між атомами, зумовлений утворенням спільних електронних пар.
Між якими частинками він реалізується? Реалізується між двома атомами внаслідок утворення однієї, двох або трьох спільних електронних пар за рахунок неспарених електронів цих атомів.
Вправа 99 / 89 (2021)
Чому не може брати участь в утворенні ковалентного зв'язку:
а) атом Магнію; Бо є атомом металічного елемента, а в утворенні ковалентного зв'язку беруть участь атоми неметалічних елементів.
б) атом Неону? Бо є атомом інертного елемента, в електронній будові якого відсутні неспарені електрони.
Вправа 90 (2021)
Серед наведених формул укажіть ті, які належать речовинам із ковалентним зв'язком: Br2, Н2О, NaBr, BaS, К2О, Ca3N2, NH3.
Ковалентний зв'язок виникає між атомами неметалічних елементів.
Вправа 100
Серед наведених формул укажіть ті, які належать речовинам із ковалентним зв'язком: І2, Н2О, NaBr, BaS, К2О, Ca3N2, NH3.
Ковалентний зв'язок виникає між атомами неметалічних елементів.
Вправа 91 (2021)
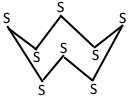
Запишіть спрощені та повні електронні формули, а також графічні формули молекул I2, SiH4 i SO3.
|
Молекулярна формула |
Спрощена електронна формула |
Повна електронна формула |
Графічна формула |
| I2 | 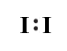 |
|
|
| SiH4 |
|
|
|
| SO3 |
|
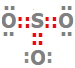 |
O=S=O ││ O |
Вправа 101
Запишіть спрощені та повні електронні формули, а також графічні формули молекул F2, Сl2O i РН3.
|
Молекулярна формула |
Спрощена електронна формула |
Повна електронна формула |
Графічна формула |
| F2 | F:F |
.. .. :F:F: .. .. |
F—F |
| Сl2O | Cl:О:Cl |
.. .. :Cl:O:Cl: .. .. |
Cl—O—Cl |
| РН3 |
H:P:H .. H |
..
H:P:H .. H |
H—P—H │ H |
Вправа 102 / 92 (2021)
Розгляньте утворення ковалентного зв'язку при сполученні двох атомів Флуору в молекулу F2.
![]()
Назвіть орбіталі, які зазнають перекривання. Перекривання зазнають 2p–орбіталі, бо в атомі Флуору на останньому енергетичному рівні міститься неспарений один р–електрон і обом атомам вигідно отримати по додатковому електрону.
Опишіть особливості цього зв'язку. У результаті зближення атомів перекриваються 2р–орбіталі атомів Флуору, утворюється спільна електронна пара за рахунок неспарених електронів цих атомів.
Вправа 103 / 93 (2021)
Охарактеризуйте хімічний зв'язок у молекулі води. В атомах Гідрогену містяться по одному s–електрону, а в атома Оксигену на зовнішньому енергетичному рівні ― шість електронів, з них, неспарені два р–електрони, тому всім атомам вигідно отримати додаткові електрони, щоб завершити свої енергетичні рівні.
У результаті зближення атомів перекриваються 1s–орбіталь кожного атома Гідрогену із 2р–орбіталлю атома Оксигену і утворюються спільні електронні пари із відповідних неспарених електронів.
Складіть схеми утворення цієї молекули з атомів Гідрогену і Оксигену, використавши спрощені та повні електронні формули частинок.
|
Н.+.О.+.Н → H:O:H
|
.. .. Н.+.О.+.Н → H:O:H .. .. |
Зобразіть графічну формулу молекули води: