Інші завдання дивись тут...
© 8next.com (відповіді, перероблене і доповнене)
Думаймо
Атом якого елемента є більш електронегативним — Оксигену чи Карбону?
Оксиген і Карбон є елементами одного періоду. У періодах зі зростанням заряду ядра атомів радіус зменшується, тому атом Оксигену має менший радіус і більший заряд ядра атома, значить сильніше притягує спільну пару електронів, отже, є більш електронегативним у порівнянні з Карбоном.
Відповідь: Оксиген.
Думаймо
Чому в таблиці б немає значень електронегативності Гелію, Неону й Аргону?
Атоми інертних елементів не здатні сполучатися з іншими атомами, а також перетворюватися на катіони чи аніони, тому нема в таблиці значень електронегативності Гелію, Неону й Аргону.
Експериментуймо
Складіть ряд усіх неметалічних елементів 1—3 періодів за збільшенням їхньої електронегативності.
Si (1,8), В (2,0), H (2,1), P (2,1), C (2,5), S (2,5), N (3,0), Cl (3,0), O (3,5), F (4,0).
Експериментуймо
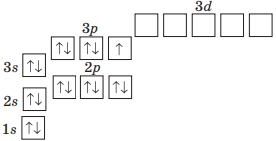
Запишіть графічний варіант електронної формули атома Хлору.
Хлор (Cl) є елементом 17 групи періодичної таблиці, тому в електронній оболонці атома на зовнішньому енергетичному рівні містить 7 електронів (…3s23s2p5).
Запишіть повну електронну і графічну формули молекули хлороводню.
| Повна електронна формула |
Графічна формула |
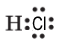 |
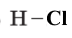 |
Думаймо
Скориставшись інформацією, наведеною в таблиці 6, укажіть формули молекул з полярним і неполярним ковалентним зв'язком.
З полярним ковалентним зв'язком формули: СO2, SF4, Сl2O7.
З неполярним ковалентним зв'язком формули: І2, РН3.
Ковалентний полярний зв'язок виникає між атомами елементів з різною електронегативністю, а неполярний — з однаковою.
Думаймо
У якій молекулі ковалентний зв'язок більш полярний — НСl чи НІ?
Обидві формули молекул містять Гідроген (2,1), тому достатньо порівняти електронегативність Хлору і Йоду. Елементи Хлор і Йод містяться в одній групі, а в групах зі зростанням заряду ядра атома електронегативність зменшується, тому Хлор (3,0) є більш електронегативний у порівнянні з Йодом (2,5). У молекулі HCl різниця електронегативності елементів дорівнює 0,9 (3,0–2,1 =0,9), а в молекулі HI — 0,4 (2,5–2,1 =0,4). Отже, значення електронегативності 0,9>0,4, тому ковалентний зв'язок більш полярний у молекулі HCl.
Відповідь: HCl.
ВИОКРЕМЛЮЄМО ОСНОВНЕ
Проаналізувавши матеріал, викладений у параграфі, запишіть у зошиті висновки про електронегативність хімічних елементів, неполярний і полярний ковалентний зв’язок.
Електронегативністю називається властивість атома зміщувати у свій бік пару електронів, спільну з іншим атомом. Електронегативність елементів у періодах зростає зліва направо, а в головних підгрупах — знизу догори. Ковалентний зв'язок, у якому одна чи кілька спільних пар електронів зміщені в бік одного з атомів, називають полярним зв'язком, а за відсутності такого зміщення — неполярним зв'язком.
Думаймо
Сформулюйте цікаве запитання за темою параграфа і поставте його своїм однокласникам/однокласницям.
У молекулі води ковалентний зв'язок полярний чи неполярний?
У молекулі води між атомом Оксигену і кожним атомом Гідрогену існує простий ковалентний зв’язок. Оскільки Оксиген має вищу електронегативність (3,5), ніж Гідроген (2,1), то його атом зміщує до себе спільні електронні пари. Отже, ковалентні зв’язки у молекулі води є полярними.
ВАШІ ДОСЯГНЕННЯ І ВІДКРИТТЯ
Вправа 365
Як впливає електронегативність атомів на хімічний зв’язок між ними?
Чим більша різниця електронегативності атомів елементів, тим полярнішим є ковалентний хімічний зв'язок.
Вправа 366
Укажіть відмінність між неполярним і полярним ковалентним зв’язком.
Ковалентний полярний і неполярний зв'язки відрізняються електронегативністю. У полярному ковалентному зв'язку різниця електронегативності атомів елементів більша від нуля, а в неполярному — дорівнює 0.
Іншими словами, у неполярному зв’язку спільна електронна пара міститься на однаковій відстані між атомами, а в полярному — зміщена в бік атома з більшою електронегативністю.
Вправа 367
Чому атоми, сполучені ковалентним зв’язком, можуть набувати невеликих зарядів?
Атоми елементів, сполучені ковалентним зв’язком, відрізняються електронегативністю. У молекулі на атомі більш електронегативного елемента з’являється надлишковий негативний заряд, а на атомі менш електронегативного елемента — позитивний.
Вправа 368
Серед наведених формул укажіть ті, що відповідають речовинам з неполярним і полярним ковалентним зв’язком: H2S, SiO2, P4, CF4, NCl3. Поясніть ваш вибір.
Речовини з неполярним зв'язком: P4, NCl3.
Речовини з полярним зв'язком: H2S, SiO2, CF4.
Поясніть ваш вибір. Ковалентний зв'язок виникає між атомами неметалічних елементів. Чим більша різниця електронегативності елементів, тим полярнішим є зв'язок між атомами, тому сполуки H2S, SiO2, CF4 з ковалентним полярним зв'язком. Якщо різниця електронегативності елементів дорівнює 0, тоді зв'язок ковалентний неполярний, тому сполука Р4, NCl3 з ковалентним неполярним зв'язком.
Вправа 369
Символи хімічних елементів часто розміщені у формулах сполук за збільшенням електронегативності елементів. Укажіть серед наведених формул такі, у яких немає зазначеної послідовності: Na2CO3, NH3, SiO2, H2S, NaOH, CH4, HNO3.
Пояснення відсутності зазаначеної послідовності:
у формулі NH3 елемент Нітроген (3,0) розташований перед Гідрогеном (2,1);
у формулі CH4 елемент Карбон (2,5) розташований перед Гідрогеном (2,1);
у формула NaOH елемент Оксиген (3,5) розташований перед Гідрогеном (2,1).
Вправа 370
Позначте часткові заряди атомів, використавши літеру δ, у формулах молекул OF2, СH4 і SiCl4. Який зв’язок у цих молекулах найбільш полярний, а який — найменш полярний?
|
О+2δ F2–δ
|
C+4δ H4–δ
|
Si+4δ Cl4–δ
|
|
Різниця електронегативності елементів у формулах:
|
|
O(3,5)
F(4,0)
4,0–3,5=0,5
|
C(2,5)
H(2,1)
2,5–2,1=0,4
|
Si(1,8)
Cl(3,0)
3,0–1,8=1,2
|
Найбільш полярний зв'язок у формулі молекули SiCl4 (різниця 1,2).
Найменш полярний зв'язок у формулі молекули CH4 (різниця 0,4).
Вправа 371*
Укажіть правильне закінчення речення «Значення електронегативності Калію та Кальцію становлять відповідно …»
а) 0,8 і 1,0;
б) 1,0 і 0,8;
в) 1,0 і 1,2;
г) 0,8 і 0,6.
Пояснення: Калій і Кальцій розташовані в одному періоді (4-му). Електронегативність елементів у періоді зростає зліва направо, тому Калій є менш електронегативний у порівнянні з Кальцієм, тому беремо до уваги варіанти а) і в). У групах електронегативність зростає знизу догори, отже, у Калію і Кальцію електронегативність менша у порівнянні з Натрієм (0,9) і Магнієм (1,2). Цим закономірностям, з двох зазначених вище варіантів, відповідає варіант а) 0,8 і 1,0.
Вправа 372
Випишіть ключові слова і словосполучення з тексту параграфа для укладання двомовного словничка.
Електронегативність — electronegativity, полярний зв'язок — polar bond, неполярний зв'язок — nonpolar bond.
Вправа 373
Створіть у зошиті таблицю оцінювання ваших знань і заповніть її.
| Навчальні досягнення (що я знаю та вмію) |
Самооцінка |
| Знаю яку властивість атома називають електронегативністю. |
... |
| Вмію визначити тип хімічного зв'язку за формулою речовини. |
... |
| Вмію визначати електронегативність елементів за шкалою Полінга. |
... |
––––––––––––– ПРОГРАМА 2016 року і 2021 року –––––––––––
§16 ПОЛЯРНИЙ І НЕПОЛЯРНИЙ КОВАЛЕНТНИЙ ЗВ'ЯЗОК. ЕЛЕКТРОНЕГАТИВНІСТЬ ЕЛЕМЕНТІВ
Вправа 104 / 94 (2021)
Чому на атомах, сполучених ковалентним зв'язком, можуть виникати невеликі заряди? Бо атоми елементів відрізняються електронегативністю. У молекулі на атомі більш електронегативного елемента з’являється надлишковий негативний заряд, а на атомі менш електронегативного елемента — позитивний.
Який ковалентний зв'язок називають полярним, а який — неполярним?
Ковалентний зв'язок, у якому одна чи кілька спільних електронних пар зміщені в бік одного з атомів, називають полярним зв'язком, а за відсутності такого зміщення — неполярним зв'язком.
Вправа 95 (2021)
Серед наведених формул укажіть ті, що відповідають речовинам із йонним, ковалентним неполярним і ковалентним полярним зв'язком: HF, СO2, MgO, Li3N, Br2, BCl3. Поясніть ваш вибір.
Йонний зв'язок виникає між атомами елементів, що різко відрізняються електронегативністю, тобто між типовими металами і типовими неметалами, тому сполуки MgO, Li3N з йонним зв'язком.
Ковалентний зв'язок виникає між атомами неметалічних елементів. Чим більша різниця електронегативності елементів, тим полярнішим є зв'язок між атомами, тому сполуки HF, СO2, BCl3 з ковалентним полярним зв'язком.
Якщо різниця електронегативності елементів дорівнює 0, тоді зв'язок ковалентний неполярний, тому сполука Br2 з ковалентним неполярним зв'язком.
Вправа 107
Серед наведених формул укажіть ті, що відповідають речовинам із йонним, ковалентним неполярним і ковалентним полярним зв'язком: HF, СO2, MgO, Li3N, Br2, NCl3. Поясніть ваш вибір.
Йонний зв'язок виникає між атомами елементів, що різко відрізняються електронегативністю, тобто між типовими металами і типовими неметалами, тому сполуки MgO, Li3N з йонним зв'язком.
Ковалентний зв'язок виникає між атомами неметалічних елементів. Чим більша різниця електронегативності елементів, тим полярнішим є зв'язок між атомами, тому сполуки HF, СO2 з ковалентним полярним зв'язком.
Якщо різниця електронегативності елементів дорівнює 0, тоді зв'язок ковалентний неполярний, тому сполуки Br2, NCl3 [N(3,0)–Cl(3,0)] з ковалентним неполярним зв'язком.
Вправа 105 / 96 (2021)
Що таке електронегативність елемента? Властивість атома елемента зміщувати у свій бік електронну пару, спільну з іншим атомом, називають електронегативністю.
Вправа 110 / 97 (2021)
Як змінюється електронегативність елементів у періодах і головних підгрупах періодичної системи? У періодах електронегативність елементів зростає зліва направо, а в головних підгрупах — знизу догори.
Вправа 109 / 98 (2021) За даними таблиці 6 складіть ряд неметалічних елементів, у якому електронегативність зменшується зліва направо.
|
F
(4,0)
|
O
(3,5)
|
Cl, N
(3,0)
|
S, C
(2,5)
|
P, H
(2,1)
|
B
(2,0)
|
Si
(1,8)
|
Вправа 106 / 99 (2021)
Використавши дані, наведені в таблиці 6, підкресліть у кожній із формул речовин символ найбільш електронегативного елемента: АlСl3, CF4, SO2, NaH, N2O5, LiOH, HClO4.
|
АlСl3
Al(1,5)
Cl(3,0)
|
CF4
C(2,5)
F(4,0)
|
SO2
S(2,5)
O(3,5)
|
NaH
Na(0,9)
H(2,1)
|
N2O5
N(3,0)
O(3,5)
|
LiOH
Li(1,0)
O(3,5)
H(2,1)
|
HClO4.
H(2,1)
Cl(3,0)
O(3,5)
|
Вправа 100 (2021)
Позначте заряди на атомах, використавши літеру δ, у таких молекулах: ОF2, CH4, SiCl4.
|
О+2δ F2–δ
|
C+4δ H4–δ
|
Si+4δ Cl4–δ
|
Який зі зв'язків у цих молекулах найбільш полярний? OF2
Який — найменш полярний? SiH4
Чим більша різниця електронегативності елементів, тим полярнішим є зв'язок між атомами, тому обчислюємо цю різницю для атомів кожної сполуки:
|
O(3,5)
F(4,0)
4,0–3,5=0,5
|
C(2,5)
H(2,1)
2,5–2,1=0,4
|
Si(1,8)
H(2,1)
2,1–1,8=0,3
|
Вправа 108
Позначте заряди на атомах, використавши літеру δ, у таких молекулах: ОF2, NH3, SCl4, SiH4.
|
О+2δ F2–δ
|
N+3δ H3–δ
|
S+4δ Cl4–δ
|
Si+4δ H4–δ
|
Який зі зв'язків у цих молекулах найбільш полярний? NH3
Який — найменш полярний? SiH4
Чим більша різниця електронегативності елементів, тим полярнішим є зв'язок між атомами, тому обчислюємо цю різницю для атомів кожної сполуки:
|
O(3,5)
F(4,0)
4,0–3,5=0,5
|
N(3,0)
H(2,1)
3,0–2,1=0,9
|
S(2,5)
Cl(3,0)
3,0–2,5=0,5
|
Si(1,8)
H(2,1)
2,1–1,8=0,3
|
Вправа 111 / 101 (2021) Укажіть правильне закінчення речення «Значення електронегативності Калію та Кальцію становлять відповідно ...»:
а) 0,8 і 1,0
б) 1,0 і 0,8
в) 1,0 і 1,2
г) 0,8 і 0,6
Візьміть до уваги і порівняйте значення електронегативності елементів, подібних до Калію і Кальцію, скориставшись таблицею 6.
У періодах електронегативність зростає зліва направо, а Калій і Кальцій є елементами одного періоду, з порядковими номерами №19 і №20 відповідно, тому електронегативність Калію менша, ніж Кальцію.
Вправа 112 / 102 (2021) Елементи в хімічних формулах сполук часто записують у порядку зростання їхньої електронегативності. Укажіть серед наведених формул такі, у яких дотримано цю послідовність: Na2CО3, NH3, SiО2, H2S, NaOH, CH4, HNО3.
Cкористайся таблицею 6.
Інші завдання дивись тут...