Інші завдання дивись тут...
© 8next.com (відповіді, перероблене і доповнене)
Відшукаймо
Дізнайтеся з інтернету про харчові продукти, які називають сублімованими.
Сублімовані продукти — це харчові продукти (фрукти, ягоди, м'ясо, овочі), зневоднені шляхом заморожування у вакуумній камері, де лід перетворюється на пару, минаючи рідку фазу.
Який процес покладено в основу їх виробництва?
Сублімаційне сушіння (ліофілізація) — це процес консервації шляхом видалення води, при якому продукт заморожується, а потім піддається вакуумному випаровуванню води зі стану льоду безпосередньо в газоподібний стан.
У чому сублімовані продукти мають перевагу порівняно зі «звичайними»?
Сублімовані продукти, у порівнянні зі «звичайними», перебувають у висушеній формі, що продовжує термін їхнього зберігання. При цьому зберігаються зовнішній вигляд та корисні властивості кінцевого продукту.
Думаймо
Молекулярні речовини в будь–якому агрегатному стані не проводять електричного струму. Поясніть цю властивість речовин, які складаються з молекул.
Молекулярні речовини не проводять електричний струм, бо в своїй структурі мають електронейтральні молекули, а не вільні носії струму — електрони чи йони.
Думаймо
Укажіть атоми Силіцію та Оксигену в моделі будови кварцу. За цією моделлю визначте валентність хімічних елементів у речовині.
У моделі будови кварцу SiO2 атоми Силіцію позначені кульками сірого кольору, а атоми Оксигену — червоного кольору. Атом Силіцію з'єднується з кожним із чотирьох атомів Оксигену, тому валентність Силіцію IV, а кожен атом Оксигену з'єднується з двома атомами Силіцію, тому валентність Оксигену II.
Обговорюймо
Наведіть приклади використання речовин з високою твердістю.
Речовинами атомної будови є алмаз і бор нітрид (BN).
Завдяки твердості алмаз використовують для різання скла та пластику, у шліфувальних кругах та в бурильних установках.
Бор нітрид за твердістю близький до алмазу і використовується для ріжучих інструментів, шліфування та полірування.
ВИОКРЕМЛЮЄМО ОСНОВНЕ
Проаналізувавши матеріал, викладений у параграфі, запишіть у зошиті висновки про найпростішу та істинну формули речовини, фізичні властивості речовин молекулярної та атомної будови.
Істинна формула показує реальний склад молекули, а найпростіша — співвідношення атомів. Речовини молекулярної будови за стандартних умов перебувають у різних агрегатних станах, мають низькі температури плавлення і кипіння, для них характерна леткість і низька твердість. Речовини атомної будови відрізняються високою твердістю, тугоплавкістю, є нелеткими і не розчиняються у воді.
Обговорюймо
Сформулюйте цікаве запитання за темою параграфа і поставте його своїм однокласникам / однокласницям.
Чому молекулярні речовини здатні до сублімації?
Молекулярні речовини за звичайних умов можуть перебувати в різних агрегатних станах завдяки слабкій міжмолекулярній взаємодії.
ВАШІ ДОСЯГНЕННЯ І ВІДКРИТТЯ
Вправа 353
Назвіть декілька речовин молекулярної та атомної будови, які ми використовуємо в побуті.
Молекулярної будови: вода, цукор, оцтова кислота, олія, нашатирний спирт, ванілін.
Атомної будови: графіт (грифлі олівців), кварцовий пісок (у складі скла), алмаз (штучний в шліфувальних інструментах).
Вправа 354
У параграфі наведено хімічну формулу оцтової кислоти СН3СООН. Це — істинна формула речовини. Чи є вона найпростішою? Якщо ні, то запишіть найпростішу формулу цієї кислоти.
Ні, формула не є найпростішою. Запишемо формулу CH3COOH у вигляді C2H4O2, індекси скоротимо на 2 і одержимо найпростішу формулу, в якій співвідношення атомів С:Н:О дорівнює 1:2:1. Отже, найпростіша формула оцтової кислоти — СН2О.
Вправа 355
Сполука Х за стандартних умов перебуває у твердому стані, має запах, а за помірного нагрівання плавиться. З яких частинок вона складається — атомів чи молекул? Сполука Х складається з молекул, бо є леткою і має низьку температуру плавлення завдяки слабкій міжмолекулярній взаємодії.
Вправа 356*
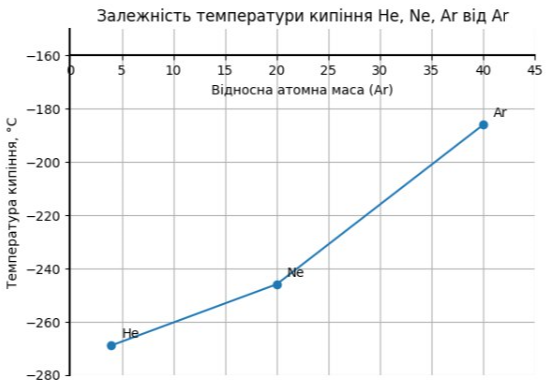
Температури кипіння рідких гелію, неону й аргону становлять –269, –246 і –186°С відповідно. Побудуйте графік залежності температур кипіння цих простих речовин від відносних атомних мас 4, 20 і 40 відповідно. Спробуйте пояснити виявлену залежність.
У ряді гелій (He), неон (Ne), аргон (Ar) збільшується відносна атомна маса від 4, 20, 40 відповідно, тому в однаковому об'ємі зменшується кількість атомів, що в свою чергу потребує меншої енергії для переходу з газоподібного стану в рідкий, тому охолоджувати треба за меншої температури по модулю.
Інертні гази — гелій, неон й аргон — мають атомну будову, але атоми в ній не сполучені між собою.
Вправа 357
Графіт і алмаз — прості речовини Карбону, які мають атомну будову, але дуже різняться твердістю. За матеріалами з інтернету з’ясуйте причину такої відмінності. Відмінність зумовлена будовою кристалічних ґраток. В алмазі кожний атом Карбону сполучений простими ковалентними зв’язками із чотирма іншими атомами. У графіті, на відміну від алмазу, атоми Карбону розташовані шарами. Всередині шару зв’язки міцні, але між шарами сили притягання слабкі, тому шари легко зсуваються, роблячи графіт м’яким. Так, коли ми пишемо олівцем, шари атомів Карбону легко відокремлюються один від одного і залишаються на папері.
Вправа 358
Чому сполуки CO2 і SiO2 істотно різняться фізичними властивостями, хоча в цих речовинах реалізується один і той самий вид хімічного зв’язку — ковалентний? Ці сполуки мають різну будову. Кварц SiO2 має атомні кристалічні ґратки, а вуглекислий газ CO2 — молекулярні кристалічні ґратки. Речовини молекулярної та атомної будови істотно різняться за фізичними властивостями.
Вправа 359
Карборунд SiC — сполука атомної будови. Спрогнозуйте фізичні властивості речовини та перевірте своє передбачення, відшукавши необхідну інформацію в інтернеті.
Карборунд SiC має бути надзвичайно твердим, тугоплавким та нерозчинним у воді та жодних розчинниках. Карборунд, як і алмаз, складається з атомів елементів 14 групи періодичної таблиці, тому має мати подібні властивості до алмазу. Довідникові дані підтверджують це передбачення. Карборунд (силіцій карбід SiC) має температуру плавлення 2830 °С і за твердістю близький до алмазу, хімічно інертний.
Вправа 360
Назвіть кілька речовин і сумішей, що мають запах і використовуються в кулінарії. З атомів чи молекул складаються ці речовини та відповідні компоненти сумішей? Ванілін, ванільний цукор, оцтова кислота, лимонна кислота, гвоздика, кориця, перець, мигдальна есенція. Ці речовини та відповідні компоненти сумішей є леткими, бо мають запах, тому складаються з молекул.
Вправа 361
У м. Брюссель (Бельгія) є монумент «Атоміум», який було споруджено до відкриття Всесвітньої виставки у 1958 р. Спробуйте пояснити назву цього монумента. Можливо запропонуєте інші назви. Назва походить від поєднання слів "атом" та "алюміній", яким спочатку були покриті сфери. Формою монумент відтворює просторове розташування атомів однієї з алотропних модифікацій заліза у формі кубічної елементарної комірки: дев'ять величезних металевих куль, діаметром 18 м, ніби зависли у повітрі, з них, вісім атомів у вершинах і один у центрі куба. Інші назви: «Алумет», «Ферум».
Вправа 362
Випишіть ключові слова і словосполучення з тексту параграфа для укладання двомовного словничка.
Молекулярна будова — molecular structure, атомна будова — atomic structure, істинна формула — true (molecular) formula, найпростіша формула — empirical formula.
Вправа 363
Створіть у зошиті таблицю оцінювання ваших знань і заповніть її.
| Навчальні досягнення (що я знаю та вмію) |
Самооцінка |
| Знаю фізичні властивості речовин молекулярної будови. |
... |
| Знаю фізичні властивості речовин атомної будови. |
... |
| Вмію передбачити фізичні властивості речовини за її будовою. |
... |
| Знаю приклади речовин, що здатні до сублімації. |
|
| Вмію визначити найпростішу формулу за істинною. |
|
––––––––– ПРОГРАМА 2016 року і 2021 року ––––––
§17 РЕЧОВИНИ МОЛЕКУЛЯРНОЇ ТА АТОМНОЇ БУДОВИ,
ЛАБОРАТОРНИЙ ДОСЛІД №1 Ознайомлення з фізичними властивостями речовин атомної, молекулярної та йонної будови
Вправа 113 / 103 (2021)
Що таке міжмолекулярна взаємодія? Явище притягання молекул одна до одної, хоча кожна є незарядженою частинкою.
Чим вона зумовлена? Силами міжмолекулярної взаємодії, так звані сили Ван–дер–Ваальса.
Вправа 114 / 104 (2021)
Сполука X за звичайних умов перебуває у твердому стані, має запах, а за слабкого нагрівання плавиться. Молекулярною чи йонною є ця сполука? Молекулярною.
Який тип хімічного зв'язку в ній реалізований? Ковалентний.
До відповіді дайте пояснення. Речовина летка й легко плавиться, тому є молекулярною сполукою.
Вправа 115 / 105 (2021)
Укажіть у поданому переліку речовини молекулярної будови: парафін, етиловий спирт, калій гідроксид, кальцій оксид, азот, олово, силіцій (ІV) оксид.
Обґрунтуйте свій вибір. Речовинам молекулярної будови властиві леткість, мала твердість, низькі температури плавлення і кипіння, не проводять електричного струму (молекули речовин не містять вільних носіїв заряду), тому це парафін, етиловий спирт і азот.
Вправа 116 / 106 (2021)
Чи можна передбачити будову речовини (йонну, молекулярну, атомну) за її зовнішнім виглядом, агрегатним станом? Відповідь поясніть. Будова речовини та її властивості пов'язані, тому якщо відома будова можна спрогнозувати властивості, і навпаки, якщо відомі властивості, можна зробити висновок про будову. Наприклад, речовини атомної будови за звичайних умов перебувають у твердому агрегатному стані, а молекулярної будови — у рідкому і газоподібному станах.
Вправа 117 / 107 (2021)
Знайдіть відповідність (позначено однаковим кольором):
|
Формула
речовини
|
Температура
плавлення, °С
|
|
1) NaH
2) НСl
|
а)+638
б) –114
|
Дайте необхідні пояснення. Натрій гідрид NaH є сполукою йонною будови, а гідроген хлорид HСl — молекулярної. Речовини йонної будови мають високі температури плавлення, а молекулярної — низькі.
Вправа 118 / 108 (2021)
Спробуйте пояснити, чому прості речовини галогени за звичайних умов перебувають у різних агрегатних станах: фтор F2 і хлор Сl2 — гази, бром Вг2 — рідина, йод І2— кристалічна речовина. Бо мають однакову будову речовин за різної температури. Йод існує у вигляді молекулярних кристалів, у вузлах ґратки — двохатомні молекули. Фтор, хлор і бром утворюють подібну будову за більш низьких температур.
Вправа 119 / 109 (2021)
Хлороводень НСl та фтор F2 мають молекули приблизно однакової маси (підтвердьте це), але істотно різняться за температурами кипіння: –84°С (НСl) та –187°С (F2). У чому, на вашу думку, причина такої відмінності?
Для підтвердження однакової маси молекул достатньо порівняти відносну молекулярну масу.
Mr(HCl)=Ar(H)+Ar(Cl)=35,5+1=36,1
Mr(F2)=2•Ar(F)=2•19=36
Чим міцніший хімічний зв'язок, що утримує частинки у вузлах кристалічних ґраток, тим міцніші кристали, тим твердіша речовина, тим вища температура її плавлення. Обидві речовини мають молекулярну будову (у вузлах молекулярної ґратки розташовані молекули), але при ковалентному неполярному зв'язку у вузлах ґратки — неполярні молекули (F2), що утримуються силами міжмолекулярної взаємодії, а при полярному зв'язку у вузлах ґратки — полярні молекули (HCl), сторого орієнтовані одна до одної своїми полюсами. Очевидно, що різним за міцністю є хімічний зв'язок: ковалентний неполярний і ковалентний полярний.
Вправа 120 / 110 (2021)
Сполука із формулою SiC має атомні кристалічні ґратки. Спрогнозуйте її фізичні властивості та перевірте ваше передбачення, знайшовши відповідну інформацію в інтернеті. Будова (тип кристалічної ґратки залежить від характеру частинок, що утворюють кристал, і від типу хімічного зв'язку між ними) речовини визначає її властивості. У вузлах атомної ґратки розміщуються атоми, сполучені ковалентними зв'язками, які є міцними, тому сполука є твердою, має дуже високі температури плавлення і кипіння, нерозчинна у воді.
Практична робота №1. Дослідження фізичних властивостей речовин.
Лабораторний дослід №1 Ознайомлення з фізичними властивостями речовин різної будови.
Реактиви: графіт, сечовина, калій бромід.
Обладнання: пробірки, шпатель, промивалка з водою, спиртівка або сухе пальне.
|
Характеристика
речовин
|
Графіт |
Сечовина |
Калій бромід |
| Будова |
атомна |
молекулярна |
йонна |
|
Тип хімічного
зв'язку
|
ковалентний
неполярний
|
ковалентний
полярний
|
йонний |
|
Фізичні властивості:
– агрегатний стан,
– колір,
– характер часточок,
– розчинність у воді,
– поведінка при
нагріванні.
|
твердий,
чорний,
кристали,
не розчиняється,
тугоплавкий
|
твердий,
білий,
кристали,
розчиняється,
легкоплавка
|
твердий,
білий,
кристали,
розчиняється,
тугоплавкий
|
Інші завдання дивись тут...