© 8next.com (відповіді, перероблене і доповнене), 2021
ЗАВДАННЯ ДЛЯ САМОКОНТРОЛЮ
Вправа 1
Ковалентний зв'язок — це зв'язок, що утворюється за рахунок спільних електронних пар.
Вправа 2
Види ковалентного зв'язку: неполярний і полярний.
Ковалентний неполярний зв'язок — це зв'язок, який утворюється між атомами з однаковою електронегативністю за рахунок спільних електронних пар, що розташовані симетрично від обох ядер атомів.
Ковалентний полярний зв'язок — це зв'язок, що утворюється між атомами з різною електронегативністю на основі спільних електронних пар.
Вправа 3.
Під час зближення двох атомів ядро першого притягує електронну орбіталь другого, а ядро другого — електронну орбіталь першого. За такої взаємодії електронні орбіталі, що містять неспарені електрони, частково перекриваються і місце перекривання електронних хмар характеризується підвищеною електронною густиною, що не дає ядрам відштовхнутися й забезпечується міцність зв'язку. Електрони перебувають у спільному користуванні двох атомів, утворюючи при цьому відповідну кількість пар спарених електронів. Електронна оболонка набуває стійкої конфігурації.
Вправа 4
Подібність між ковалентним неполярним і ковалентним полярним зв'язками: хімічні зв'язки утворюються за рахунок спільних електронних пар, виникають між атомами неметалічних елементів.
Відмінність між ковалентним неполярним і ковалентним полярним зв'язками: різними є зміщення електронних пар і значення електронегативності атомів елементів.
Вправа 5
а) неполярний зв'язок: F2, O2, I2, N2
б) полярний зв'язок: HF, H2SO4, NH3, H2S
Ковалентний зв'язок виникає між атомами неметалічних елементів. Неполярний зв'язок виникає між атомами однакових хімічних елементів, а полярний — між атомами різних хімічних елементів.
Вправа 6
а) ковалентний неполярний зв'язок.
|
сполука валентність елемента |
F2
І |
O2
ІІ |
I2
І |
N2
ІІІ |
|
електронна формула |
.. .. :F:F: .. .. |
:O::O: .. .. |
.. .. :I:I: .. .. |
:N::N: .. |
|
структурна формула |
F—F | О=О | І—І | NΞN |
б) ковалентний полярний зв'язок.
|
сполука валентність елементів |
HF І і І |
H2SO4 І, VI, II |
NH3 III i I |
H2S I i II |
|
електронна формула |
.. H:F: .. |
O :: H:O:S:O:H :: O |
.. H:N:H: .. N |
.. H:S:H .. |
|
структурна формула |
H—>F |
H—O O \ ̸ ̸ S ̸ \\ H—O O |
H ↓ H—>N<— H |
H—>S<—H |
Пояснення. Покажемо як складати структурну (графічну) формулу на прикладі кислоти H2SO4.
Сульфур у кислоті шестивалентний, тому записуємо навколо цього кислотворного елемента шість рисок:
\ /
— S —
̸ \
Усі ці риски мають належати чотирьом двовалентним атомам кисню. Розміщуємо всі атоми Оксигену навколо атома Сульфура, причому двом з них виділяємо по дві риски, а двом залишається по одній рисці.
О О
\ //
S
̸ \\
О О
Двом атомам Оксигену не вистачає по одній рисці (Оксиген — двовалентний елемент), тому проводимо їх і дописуємо зліва до кожної з них атом Гідрогену.
Н— О О
\ //
S
̸ \\
Н—О О
Вправа 7
а) двох s-орбіталей; Н2
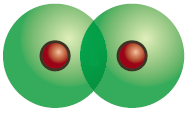
б) s- і р-орбіталей (за будь-якою з осей х, у, z); HCl, HF, HI.
