СТОРІНКА 58
Заняття 28
Фізичні та хімічні явища
Вправа 1
Утворення рум'яної скоринки на булочці – це хімічне явище.
Вправа 3
Опорний конспект до теми. Запишіть визначення понять і наведіть приклади.
| Явище | |
| Фізичне | Хімічне |
|
Явище, під час перебігу якого не відбувається змін хімічного складу речовин. |
Явище, під час перебігу яких одні речовини перетворюються на інші. |
|
Замерзання води, утворення інею, плавлення алюмінію, танення льоду, плавлення цукру, утворення сніжинок, розшарування олії з водою, світіння лампочки, поширення запаху ефіру, фільтрування. |
Іржавіння заліза, горіння бензину, прокисання молока, згоряння палива в двигуні, горіння свічки, вибух динаміту, бродіння виноградного соку, псування продуктів харчування, гниття органічних рештків, утворення нальоту на мідних предметах. |
Укажіть, які фізичні явища супроводжують процеси горіння.
| Випромінювання світла |
Горіння свічки |
Виділення тепла |
Робота в групах
Складіть із виділених літер слова та впишіть їх у клітинки.
ХІМІЯ ЦІКАВА НАУКА
СТОРІНКА 59
Вправа 6
Хімічні явища: згорів аркуш паперу, старий автомобіль почав іржавіти, бензин горить дуже яскраво.
СТОРІНКА 60
Заняття 29
Моделювання фізичних і хімічних явищ
Вправа 2
Правдиві ("+") чи ні ("–") твердження.
1 +
2 – (хімічне явище)
3 +
4 – (фізичне явище)
5 – (фізичне явище)
6 +
7 +
8 +
9 – (фізичне явище)
Вправа 3
1. Моделюємо вивердження вулкану.
Запишіть спостереження.
Спостерігаємо хімічну реакцію, що супроводжується бурхливим виділенням піни, яка виливається, імітуючи лавовий потік.
СТОРІНКА 62
Заняття 30
Хімічні реакціі. Схема хімічної реакції
Вправа 1
У космосі відбуваються хімічні реакції.
Вправа 2
Правдиві ("+") чи ні ("–") твердження.
1 +
2 +
3 +
4 – (фізичне явище)
5 – (за допомогою фізичних способів розділення суміші)
6 +
7 – (неоднорідна суміш)
8 – (фізичне явище)
9 +
Вправа 3
Опорний конспект до теми
Хімічні реакції — це явища перетворення одних речовин на інші.
Схема хімічної реакції — це умовний запис процесу перебігу хімічної реакції.
Вихідні речовини (реагенти) — речовини, які беруть участь в хімічній реакції.
Продукти реакції — речовини, які утворюються в результаті.
Індекс — позначає кількість атомів або групи атомів у хімічній формулі.
Коефіцієнт — позначають кількість молекулів або формульних одиниць у хімічній формулі.
Вправа 4
Зовнішні ефекти перебігу хімічних реакцій: поява/зникнення запаху, зміна забарвлення, виділення газу, утворення осаду.
| Коефіцієнти | ||
| 2H2CO3 | 5Ca(OH)2 | 4CO(NH2)2 |
| Індекси | ||
СТОРІНКА 63
Заповніть таблицю за зразком
|
Хімічний запис |
Кількість молекул |
Хімічні елементи |
Кількість атомів кожного елемента |
| 4K2MnO4 | 4 | K, Mn, O | K – 8, Mn – 4, O – 16 |
| 10Na3PO4 | 10 | Na, P, O | Na – 30, P – 10, O – 40 |
| 7Ba(NO3)2 | 7 | Ba, N, O | Ba – 7, N – 14, O – 42 |
| NH4OH | 1 | N, H, O | N – 1, H – 5, O – 1 |
Вправа 4
Укажіть номери реакцій, у яких
виділяється газ: 2, 3, 5, 7, 11, 14
утворюється нерозчинна рідина: 4, 10,12, 13
реагентами є лише складні речовини: 3, 6, 7, 8, 9, 10, 12, 14
серед реагентів є проста речовина: 2, 5,11, 15
утворюються дві складні речовини: 7, 8, 10, 12
реагенти є простими речовинами: 1, 4, 13
Вправа 5
Розгадайте кросворд
По горизонталі
1. коефіцієнт
3 схема
5 реагенти
По вертикалі
2. осад
4. продукти
6 індекс
7 хімічні
СТОРІНКА 64
Заняття 31
Типи хімічних реакцій
Вправа 1
Зі складної речовини може утворитися проста речовина, внаслідок реакції розкладу.
Вправа 2
Правдиві ("+") чи ні ("–") твердження.
1 +
2 – (під час фізичних явищ)
3 +
4 +
5 – (продукти реакції)
6 +
7 +
8 – (складні і прості речовини)
9 +
Вправа 3
Увідповіднили однаковим кольором
| Тип реакції | Опис | Приклад |
| Cполучення |
У результаті складні речо– вини обмінюються своїми складовими. |
K + Cl2 → KCl |
| Заміщення |
З двох і більше реагентів утворюється один продукт реакції. |
CaCO3 → CaO + CO2 |
| Розкладу |
У результаті реакції атоми простої речовини заміщу– ють атоми іншого елемен– та в складній речовині. |
Mg + HCl → MgCl2 + H2 |
| Обміну |
З одного реагента утворю– ються два й більше про– дукти реакції. |
BaCl2 + MgSO4 → BaSO4 + MgCl2 |
СТОРІНКА 65
Вправа 4
1. Внесіть у пробірку шпателем порошок соди та обережно вилийте декілька крапель розчину хлоридної кислоти. Що спостерігається?
Бурхливо виділяється газ (вуглекислий газ СО2)
2. Налийте в пробірку 1 мл розчину гідроген пероксиду та обережно пінцетом внесіть шматочок сирої картоплі. Що спостерігається?
Активно вспінюється зріз картоплі, внаслідок виділення газу (кисню О2).
3. Налийте в пробірку 1 мл розчину купрум(ІІ) сульфату та обережно додайте декілька крапель розчину натрій гідроксиду. Що спостерігається?
Утворюється яскраво–блакитний осад (Cu(OH)2).
| Рівняння реакції | Тип реакції |
| 1. NaHCO3 + HCl → NaCl + H2O + CO2↑ | реакція обміну |
| 2. H2O2 → H2O + O2 | реакція розкладу |
| 3. CuSO4 + NaOH → Cu(OH)2 + Na2SO4 | реакція обміну |
Вправа 5
Спостерігали реакцію "гасіння" соди.
Вихідними речовинами є питна сода NaHCO3 і розчин етанової (оцтової) кислоти СН3СООН.
Схема реакції:
NaHCO3 + CH3COOH → CH3COONa + CO2↑ + H2O
Тип реакції: реакція обміну.
Чому сода має розпушувальну дію? Утворюється газоподібна речовина — вуглекислий газ CO2.
Вправа 6
Підбиваємо підсумки
Ментальна карта "Типи хімічних реакцій"
| Типи хімічних реакцій | |||
|
↓ сполучення |
↓ розкладу |
↓ заміщення |
↓ обміну |
СТОРІНКА 66
Заняття 32
Хімічні рівняння.
Закон збереження маси в хімічних реакціях
Вправа 1
Чим відрізняється хімічне рівняння від схеми.
Хімічне рівняння відрізняється від схеми реакції тим, що кількість атомів кожного елемента в лівій і правій його частинах однакова, що узгоджується із законом збереження маси реагентів і продуктів реакції, тому замість стрілки ставиться знак «дорівнює».
Вправа 2
Правильні твердження?
Проста речовина містить атоми одного хімічного елемента. ТАК
За кількістю та складом реагентів і продуктів реакції є 4 типи реакцій. ТАК
Утворення води та кисню з гідроген пероксиду є реакцією заміщення. НІ
Індекси – числа, що вказують на кількість молекул або формульних одиниць. НІ
У реакціях сполучення єдиним реагентом є складна речовина. НІ
Нерозчинну речовину у схемі реакції позначають "↓" біля її формули. ТАК
Реагенти – речовини, які утворюються в результаті реакції. Ні
Лише складні речовини здатні до розкладу. ТАК
У реакції сполучення єдиним реагентом є складна речовина. НІ
Вправа 3
Опорний конспект до теми.
Закон збереження маси речовин:
маса реагентів = маса продуктів реакції
Хімічне рівняння — це запис хімічної реакції за допомогою хімічних формул реагентів і продуктів, який відповідає закону збереження маси речовин.
Кількість атомів кожного елемента в реагентах повинна дорівнювати кількості його атомів у продуктах реакції.
Тому доцільно перетворювати схеми хімічних реакцій на рівняння, додаючи коефіцієнти.
| Реакція | Сума коефіцієнтів | Тип реакції |
| 2KOH + SO3 = K2SO4 + H2O | 5 | заміщення |
| 2HCl + Fe = FeCl2 + H2 | 5 | заміщення |
| 2Al + 2NH3 = 2AlN + 3H2 | 9 | заміщення |
| 4Fe + 3O2 = 2Fe2O3 | 9 | сполучення |
| Al2O3 + 2KOH = 2KAlO2 + H2O | 6 | заміщення |
| H3PO4 + 3AgNO3 = Ag3PO4 + 3HNO3 | 8 | обміну |
| N2O5 + 2NaOH = 2NaNO3 + H2O | 6 | заміщення |
| 3MgSO4 + 2Na3PO4 = Mg3(PO4)2 + 3Na2SO4 | 9 | обміну |
| AlBr3 + 3NaOH = Al(OH)3 + 3NaBr | 8 | обміну |
Схема реакції фотосинтезу: CO2 + H2O → C6H12O6 + O2↑
Процес фотосинтезу відбувається у зелених частинах рослин (переважно листках), а органелах клітин — хлоропластах, що містять зелений пігмент хлорофіл.
СТОРІНКА 67
Вправа 4
Робота в парах
2. Маса речовин унаслідок хімічних реакцій лишається незмінною.
3. Дослідіть явища горіння паперу та іржавіння заліза.
| Явище |
Горіння паперу |
Іржавіння заліза |
| Гіпотеза |
Унаслідок горіння паперу молекули реагують з киснем з навколишнього середовища, утворюючи попіл, маса якого менша, ніж маса початкового паперу, бо в повітря виді- ляється газ. |
У разі іржавіння заліза атоми Феруму реагують з киснем і водою з навколишнього повітря, утворюючи іржу, маса якої більша, ніж маса початкового заліза.
|
|
План експерименту |
1. Зважуємо папір. 2. Спалюємо папір. 3. Зважуємо отриманий попіл. 4. Порівнюємо значення мас. |
1. Зважуємо залізо 2. Прожарюємо залізо. 3. Зважуємо прожарене залізо. 4. Порівнюємо значення мас. |
|
Очікуванні результати |
Маса має зменшитися.
|
Маса має збільшитися.
|
| Спостереження | Виділяється газ і папір чорніє. | Метал чорніє. |
| Висновки |
Маса зменшилася за рахунок виділення газу. |
Маса збільшилася за рахунок утворення іржі. |
Вправа 6
Нашу гіпотезу підтверджено.
СТОРІНКА 68
Заняття 33
Складання хімічних рівнянь
Вправа 1
Яка різниця між коефіцієнтом та індексом?
Коефіцієнтом позначають кількість молекулів або формульних одиниць у хімічній формулі, а індекс — кількість атомів або групи атомів.
Вправа 2
Правдиві ("+") чи ні ("–") твердження.
1 – (запис рівняння)
2 +
3 +
4 – (однакова)
5 – (коефіцієнти)
6 – (дорівнює 1)
7 – (на кількість молекул або формульних одиниць)
8 – (хімічних явищ)
9 +
Вправа 3
1. зрівнюємо кількість атомів, розтавляючи коефіцієнти в лівій і правій частинах рівняння.
2. кількість атомів кожного елемента в обох частинах схеми.
3. то закон збереження маси виконується.
4. на знак рівності.
5. зрівняні.
СТОРІНКА 69
Вправа 5
1) Запишіть схемку реакції розкладу кальцій гідрогенкарбонату та перетворіть його на рівняння реакції.
Ca(HCO3)2 → CaCO3↓ + CO2↑ + H2O
2Ca(HCO3)2 = 2CaCO3↓+ CO2↑ + H2O
2) Обчисли масу кальцій гідрогенкарбонату (г), що містився в 1 л води, після кип'ятіння якої утворилося 300 мг осаду, 54 мг води та виділилося 132 мг газу.
Відомо: m(CaCO3)=300 мг, m(H2O)=54 мг, m(CO2)=132 мг
Знайти: m(Ca(HCO3)2)–?
Розв'язання
m(Ca(HCO3)2) = m(CaCO3) + m(H2O) + m(CO2) = 300 мг + 54 мг + 132 мг = 486 мг
Відповідь: 486 мг.
3) Рівняння реакції розкладу магній гідрогенкарбонату.
2Mg(HCO3)2 = 2MgCO3↓ + CO2↑ + H2O
Вправа 7
Уставте пропущені слова.
А. Лаувазьє,
вихідних речовин, реакції,
закритих, елементи,
зберігаються,
рівняння, коефіцієнти.
СТОРІНКА 70
Заняття 34
Проєктна діяльність
Вправа 2
Рівняння реакції:
2H2O2 = 2H2O + O2↑
Правдиві ("+") чи ні ("–") твердження.
1 – (реакція розкладу)
2 – (реагентом є пероксид водню)
3 +
4 +
5 +
6 +
7 – (сума коефіцієнтів у правій частині дорівнює 3)
8 +
9 +
СТОРІНКА 72
Заняття 35
Підсумковий урок. Гра "Хімічний марафон"
Вправа 1
Асоціативний кущ поняття хімія.
1. речовини
2. молекули, атоми
3. хімічні елементи (118 у періодичній таблиці)
4. хімічні реакції
5. лабораторне обладнання
6. перетворення та властивості
Вправа 2
Зупинка 1. Історична
Історія відкриття хімічного елемента Натрій.
Натрій був уперше виділений англійським хіміком Гамфрі Деві у 1807 році шляхом електролізу розплавленого гідроксиду натрію (NaOH). Це відкриття дозволило отримати новий сріблясто–білий, м'який метал, який швидко тьмяніє на повітрі та бурхливо реагує з водою.
Походження назви цього елемента.
Назва хімічного елемента Натрій походить від араб, «натр» – сода.
Зупинка 2. Періодична.
а) Кадмій, порядковий номер 48, 5–ий період, 12 група.
б) Калій, порядковий номер 19, 4–ий період, 1 група.
Зупинка 3. Прості речовини.
Приклади хімічних елементів, назви яких відрізняються від від назв простих
Гідроген, Карбон, Нітроген, Оксиген, Флуор, Сульфур, Ферум, Купрум, Аргентум, Станум, Аурум, Меркурій, Плюмбум.
Зупинка 4. Загадкова
Розшифруйте анаграми
|
ОКСИГЕН НІТРОГЕН СУЛЬФУР |
МАГНІЙ КУПРУМ АУРУМ |
АЛЮМІНІЙ ФОСФОР ЙОД |
СТОРІНКА 73
Зупинка 5. Ерудитна
Os – Осмій
В – Бор
Br – Бром
F – Флуор
N – Нітроген
Dy – Диспрозій
Lv – Лівермоній
Зупинка 6. Суміші
Послідовність розділення:
1) суміші залізних ошурків, піску та кухонної солі.
Дією магніту вибрати залізні ошурки, долити води для відстоювання, фільтруванням вибрати пісок, а випарюванням одержимо сіль.
2) суміші тирси, спирту та води.
Фільтруванням вибрати тирсу, випарюванням одержимо сіль, конденсацією пари отримаємо воду.
Зупинка 7. Модельна
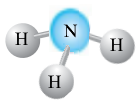
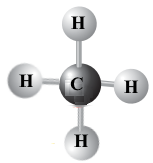
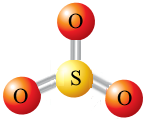
Пропонуємо моделі сполук CO2, NH3, CH4, SO3.
 |
 |
 |