Інші завдання дивись тут...
© 8next.com (відповіді, перероблене і доповнене)
Виконаймо вправу
Доведіть валентність Сульфуру в оксиді SO2, склавши спрощену електронну формулу молекули речовини та її графічну формулу.
| Спрощена електронна формула |
Графічна формула |
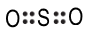 |
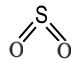 |
Спільна електронна пара у спрощеній електронній формулі позначається двома крапками, таких пар крапок є 4, а в графічній — рискою, таких рисок є 4.
Валентність атома в молекулі можна визначити за кількістю пар крапок (спільних електронних пар) у електронній формулі і за кількістю рисок у графічній формулі.
Таких пар крапок у спрощеній електронній формулі є 4 і в графічній — 4. Отже, валентність Сульфуру в оксиді SO2 дорівнює IV.
Виконаймо вправу
Доведіть, що Фосфор може бути три- і п'ятивалентним, зобразивши зміну будови його атома за допомогою електронних формул.
У звичайному стані атом Фосфору (15 група) на зовнішньому енергетичному рівні має 5 електронів, з яких, два спарені і три неспарені (...3s23p3).
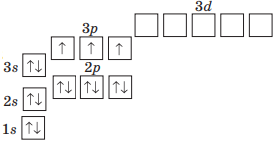
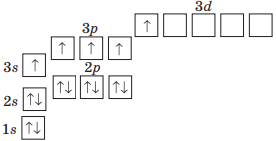
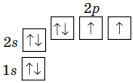
Поглинаючи певну порцію енергії, атом Фосфору змінює свою електронну будову. Один електрон переміщується із 3s-орбіталі у вільну 3d-орбіталь, унаслідок чого кількість неспарених електронів в атомі збільшується до п'яти (...3s13d13p3).
Кількість неспарених електронів в атомі вказує на можливе значення валентності елемента, тому Фосфор може бути три- і п'ятивалентним.
Думаймо
Чому значення валентності Cульфуру парні, а Фосфору і Хлору — непарні?
У періодичній таблиці Сульфур перебуває в VI групі, номер групи є парним числом, тому атом для досягнення октету (8), віддає або приєднує парну кількість неспарених електронів, отже, значення валентності Сульфуру — парні.
У періодичній таблиці Фосфор і Хлор перебувають у V і VII групах відповідно, номери цих груп є непарними числами, тому атом для досягнення октету (8), віддає або приєднує непарну кількість неспарених електронів, отже, значення валентності Фосфору і Хлору — непарні.
Виконаймо вправу
Визначте валентність Хлору у сполуках Сl2O і Сl2O7.
У сполуці Cl2O валентність Оксигену стала і дорівнює ІI. Обчислюємо валентність усіх атомів Оксигену (2•1=2) і ділимо на число атомів Хлору (2:2=1). Валентність Хлору — I.
У сполуці Cl2O7 валентність Оксигену стала і дорівнює ІI. Обчислюємо валентність усіх атомів Оксигену (2•7=14) і ділимо на число атомів Хлору (14:2=7). Валентність Хлору — VII.
Виконаймо вправу
Бор — тривалентний елемент. Наведіть електронну формулу, яку має його атом, сполучаючись з іншими атомами.
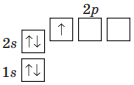
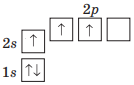
У звичайному стані атом Бору (13 група) на зовнішньому енергетичному рівні має 3 електрони, з яких, два спарені і один неспарений (...2s22p1), тому валентність Бору дорівнює I.
Поглинаючи певну порцію енергії, атом Бору змінює свою електронну будову. Один електрон переміщується із 2s-орбіталі у вільну 2р-орбіталь, унаслідок чого кількість неспарених електронів в атомі збільшується до трьох (...2s12p2), тому валентність Бору дорівнює III.
Повна електронна формула атома Бору, де Бор — тривалентний елемент:1s22s12p2
Складіть хімічні формули сполук Бору із Флуором та Оксигеном.
У сполуках Бор має валентність III, Флуор — I, Оксиген — II.
Складаємо формулу сполуки Бору з Флуором.
Записуємо хімічні символи елементів, над ними позначаємо валентність елементів: BIIIFI. Найменше спільне кратне валентностей обох елементів дорівнює три. Отримане число ділимо на величину валентності кожного з елементів (3:3=1 i 3:1=3) — це індекси, які ставимо біля символу відповідного хімічного елемента (на письмі 1 не пишемо). Отже, формула BF3.
Складаємо формулу сполуки Бору з Оксигеном.
Записуємо хімічні символи елементів, над ними позначаємо валентність елементів: BIIIOII. Найменше спільне кратне валентностей обох елементів дорівнює шість. Отримане число ділимо на величину валентності кожного з елементів (6:3=2 i 6:2=3) — це індекси, які ставимо біля символу відповідного хімічного елемента. Отже, формула B2O3.
ВИОКРЕМЛЮЄМО ОСНОВНЕ
Проаналізувавши матеріал, викладений у параграфі, запишіть у зошиті висновки про валентність хімічних елементів, з’ясування її значення за формулою сполуки і складання формули сполуки за валентністю елементів, якими вона утворена.
Валентність — це здатність атома утворювати хімічні зв’язки. Валентність визначається кількістю неспарених електронів. Максимальна валентність дорівнює номеру групи, в якій перебуває елемент, відняти 10. Валентність елемента у бінарній сполуці можна визначити за відомою валентістю іншого елемента у цій сполуці. Для складання формули бінарної сполуки за відомими валентностями елементів, потрібно знайти найменше спільне кратне (НСК) цих валентностей і поділити це число на валентність кожного елемента, щоб отримати значення індексів.
ДУМАЙМО
Сформулюйте цікаве запитання за темою параграфа і поставте його своїм однокласникам/однокласницям.
Чому валентність Оксигену постійна і дорівнює II?
Це пояснюється будовою атома. В електронній оболонці атома Оксигену відсутні вільні орбіталі, тому неможливим є розпаровування електронів, щоб збільшити валентність. Зовнішній енергетичний рівень атома Оксигену містить два неспарені електрони, тому валентність Оксигену дорівнює II.
ВАШІ ДОСЯГНЕННЯ І ВІДКРИТТЯ
Вправа 344
Як визначити валентність атома в молекулі за її графічною та електронною формулами?
Валентність атома в молекулі можна визначити за кількістю рисок у графічній формулі і за кількістю пар крапок (спільних електронних пар) у скороченій електронній формулі.
Вправа 345
Які значення валентності може мати хімічний елемент, якщо електронна формула його атома — 1s22s22p63s23p2?
У звичайному стані атом хімічного елемента на зовнішньому енергетичному рівні на 3р-орбіталі має 2 неспарені електрони, тому валентність II. Коли атом цього хімічного елемента поглинає порцію енергії, і один зі спарених електронів із 3s-орбіталі переміщується в 3р-орбіталь, тоді кількість неспарених електронів збільшується до 4-х і валентність дорівнює IV.
Отже, хімічний елемент може мати валентність: II і IV.
Вправа 346
Допишіть значення валентності хімічних елементів у формулах сполук: SIVCl4, PBr5I, NI3I, CIVS2, P3N5III
Відповідь: SIVCl4I, PVBr5I, NIIII3I, CIVS2II, P3VN5III.
У сполуці SCl4 обчислюємо валентність усіх атомів Сульфуру (1•4=4) і ділимо на число атомів Хлору (4:4=1). Валентність Хлору — I.
У сполуці PBr5 обчислюємо валентність усіх атомів Брому (5•1=5) і ділимо на число атомів Фосфору (5:1=5). Валентність Фосфору — V.
У сполуці NI3 обчислюємо валентність усіх атомів Йоду (3•1=3) і ділимо на число атомів Нітрогену (3:1=3). Валентність Нітрогену — IІІ.
У сполуці CS2 обчислюємо валентність усіх атомів Карбону (4•1=4) і ділимо на число атомів Сульфуру (4:2=2). Валентність Сульфуру — IІ.
У сполуці P3N5 обчислюємо валентність усіх атомів Нітрогену (3•5=15) і ділимо на число атомів Фосфору (15:3=5). Валентність Фосфору — V.
Вправа 347
Визначте валентність елементів у сполуках, що мають такі формули:
а) V2O5, SiF4, PH3;
Відповідь: V2VO5II, SiIVF4I, PIIIH3I
У сполуці V2О5 валентність Оксигену — ІI. Обчислюємо валентність усіх атомів Оксигену (2•5=10) і ділимо на число атомів Ванадію (10:2=5). Валентність Ванадію — V.
У сполуці SiF4 валентність Флуору — І. Обчислюємо валентність усіх атомів Флуору (1•4=4) і ділимо на число атомів Силіцію (4:1=4). Валентність Силіцію — IV.
У сполукаці PH3 валентність Гідрогену — І. Oбчислюємо валентність усіх атомів Гідрогену (1•3=3) і ділимо на число атомів Фосфору (3:1=3). Валентність Фосфору — IІІ.
б) H2Se, P2O3, Mn2O7.
Відповідь: H2ISeII, P2IIIO3II, Mn2VIIO7II.
У сполуці H2Se валентність Гідрогену — І. Обчислюємо валентність усіх атомів Гідрогену (1•2=2) і ділимо на число атомів Селену (2:1=2). Валентність Селену — II.
У сполуці P2О3 валентність Оксигену — ІI. Обчислюємо валентність усіх атомів Оксигену (2•3=6) і ділимо на число атомів Фосфору (6:2=3). Валентність Фосфору — III.
У сполуці Mn2О7 валентність Оксигену — ІI. Обчислюємо валентність усіх атомів Оксигену (2•7=14) і ділимо на число атомів Мангану (14:2=7). Валентність Мангану — VII.
Вправа 348
а) SiIV..H.., WVI..O.., O..F; Відповідь: SiH4, WO3, OF2.
Записуємо хімічні символи елементів, над ними позначаємо валентність елементів: SiIVHI. Найменше спільне кратне валентностей обох елементів дорівнює чотири (4•1=4). Отримане число ділимо на величину валентності кожного з елементів (4:4=1 i 4:1=4) — це індекси, які ставимо біля символу відповідного хімічного елемента (на письмі 1 не пишемо). Отже, формула SiH4.
Записуємо хімічні символи елементів, над ними позначаємо валентність елементів: WVIOII. Найменше спільне кратне валентностей обох елементів дорівнює шість. Отримане число ділимо на величину валентності кожного з елементів (6:6=1 i 6:2=3) — це індекси, які ставимо біля символу відповідного хімічного елемента (на письмі 1 не пишемо). Отже, формула WO3.
Записуємо хімічні символи елементів, над ними позначаємо валентність елементів: OIIFІ. Найменше спільне кратне валентностей обох елементів дорівнює два (2•1=2). Отримане число ділимо на величину валентності кожного з елементів (2:2=1 i 2:1=2) — це індекси, які ставимо біля символу відповідного хімічного елемента (на письмі 1 не пишемо). Отже, формула OF2.
б) NIII..O..,PV..O..,CIV..Cl... Відповідь: N2O3, P2O5, CCl4.
Записуємо хімічні символи елементів, над ними позначаємо валентність елементів: NIIIOІI. Найменше спільне кратне валентностей обох елементів дорівнює шість (3•2=6). Отримане число ділимо на величину валентності кожного з елементів (6:3=2 i 6:2=3) — це індекси, які ставимо біля символу відповідного хімічного елемента. Отже, формула N2O3.
Записуємо хімічні символи елементів, над ними позначаємо валентність елементів: PVOІI. Найменше спільне кратне валентностей обох елементів дорівнює десять (5•2=10). Отримане число ділимо на величину валентності кожного з елементів (10:5=2 i 10:2=5) — це індекси, які ставимо біля символу відповідного хімічного елемента. Отже, формула P2O5.
Записуємо хімічні символи елементів, над ними позначаємо валентність елементів: CIVClI. Найменше спільне кратне валентностей обох елементів дорівнює чотири (4•1=4). Отримане число ділимо на величину валентності кожного з елементів (4:4=1 i 4:1=4) — це індекси, які ставимо біля символу відповідного хімічного елемента (на письмі 1 не пишемо). Отже, формула ССl4.
Вправа 349
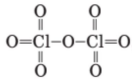
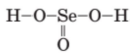
Визначте валентність елементів у сполуках за графічними формулами молекул:
|
Графічна
формула
|
H–N=C=S |
|
|
|
Валентність
елементів
|
H (I)
N (III)
C (IV)
S (II)
|
Cl (VII)
O (II)
|
H (I)
O (II)
Se (IV)
|
Вправа 350
Чому в книжках та інтернеті немає відомостей про валентність Гелію, Неону, Аргону?
Прогнозувати валентність хімічного елемента можна, узявши до уваги кількість неспарених електронів у його атомі. Атоми хімічних елементів Гелію, Неону, Аргону на останньому енергетичному рівні мають усі електрони спарені, тому говорити про валентність цих хімічних елементів не можна. Ось чому в книжках та інтернеті немає відомостей про валентність Гелію, Неону, Аргону.
Вправа 351
Випишіть ключові слова і словосполучення з тексту параграфа для укладання двомовного словничка.
Валентність — valence, одновалентний — univalent, двовалентний — divalent, трьохвалентний — trivalent, чотирьовалентний — tetravalent, змінна валентність — valence variables, постійна валентність — constant valence.
Вправа 352
Створіть у зошиті таблицю оцінювання ваших знань і заповніть її.
| Навчальні досягнення (що я знаю та вмію) |
Самооцінка |
| Знаю, яку властивість атома називають валентністю. |
... |
| Знаю, як визначити валентність хімічного елемента. |
... |
| Вмію складати хімічну формулу бінарної сполуки. |
... |
| Вмію визначати валентність елементів у хімічній формулі бінарної сполуки. |
...
|
––––––––– ПРОГРАМА 2021 року ––––––––––
§8 ПЕРІОДИЧНИЙ ЗАКОН І ЕЛЕКТРОННА БУДОВА АТОМІВ
Вправа 46
Поступово чи періодично змінюється зі зростанням порядкового номера елемента:
а) загальна кількість електронів в атомі? Поступово
б) кількість електронів на зовнішньому енергетичному рівні? Періодично
Вправа 47
Випишіть у стовпчик усі символи елементів, що починаються з літери N. Після кожного символу вкажіть назву і тип відповідного елемента (s-, р-, d- чи f-елемент).
| Символ |
Назва |
Тип елемента |
|
N
Ne
Na
Ni
Nb
Nd
Np
No
|
Нітроген
Неон
Натрій
Нікель
Ніобій
Неодим
Нептуній
Нобелій
|
p-елемент
p-елемент
s-елемент
d-елемент
d-елемент
f-елемент
f-елемент
f-елемент
|
Клітинки елементів у періодичній системі мають певний колір — рожевий (s-елементи), жовтий (р-елементи), синій (d-елементи), зелений (f-елементи).
Вправа 48
Елементам яких типів належать такі електронні формули атомів:
а) 1s22s22p63s2; s-елемент
б) 1s22s22p1; p-елемент
в) 1s22s22p63s23p4? p-елемент
Назва орбіталі, що заповнюється останньою, визначає назву електрона (елемента).
Вправа 49
Не складаючи електронних формул, укажіть кількість електронів на останньому енергетичному рівні в атомах:
Cl — сім
Pb — чотири
As — п'ять
Кг — вісім
Номер групи, в якій міститься елемент, для елементів головних підгруп вказує на кількість електронів на останньому енергетичному рівні.
Вправа 50 Назвіть кілька хімічних елементів, максимальне значення валентності яких дорівнює 7.
Елементи VII групи: Хлор, Бром, Йод (окрім Флуору)
Вправа 51
Укажіть можливі значення валентності хімічного елемента, якщо електронна формула його атома:
а) 1s22s22p63s23p3
Можлива валентність III і вища валентність V елемента Фосфора, що розміщується в V групі головній підгрупі Періодичної системи.
б) [Ne]3s23p5
Можливі валентності I, III, V і вища валентність VII елемента Хлор, що розміщується в VII групі головній підгрупі Періодичної системи.
Інші завдання дивись тут...